曜点回顾 | 东曜药业生物制剂技术转移关键考量点分享
近日,第15届弗戈制药工程国际论坛于南京举办,东曜药业偶联及制剂生产负责人周昀总监出席“生物制药工程与工艺分论坛”,分享了“生物制剂技术转移关键考量点”的主题报告。
生物制剂的技术转移是项目前期的关键步骤,也是推进项目顺利开展的基础。这一步骤的成功进行也有助于增强CDMO客户的信心。
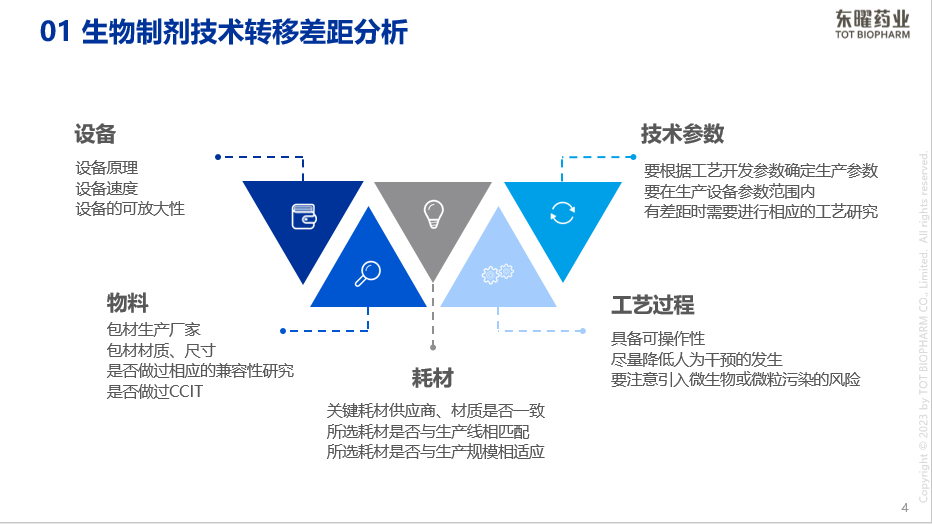
生物制剂技术转移的第一步即为差异分析,周昀总监从设备、物料、耗材、工艺过程和技术参数五个方面详细阐释了如何将差异控制在可接受的范围内,以使技术转移顺利实现。
随着项目的展开,工艺和GMP两大模块是生物制剂技术转移的关键组成。在工艺中,从化冻到灌装、冻干等各个细节都需要考量;比如化冻的方式、温度、过程等不同因素如何选择,冻干设备、工艺、过程控制等多个方面如何操作,都决定了技术转移工作能否顺利开展。
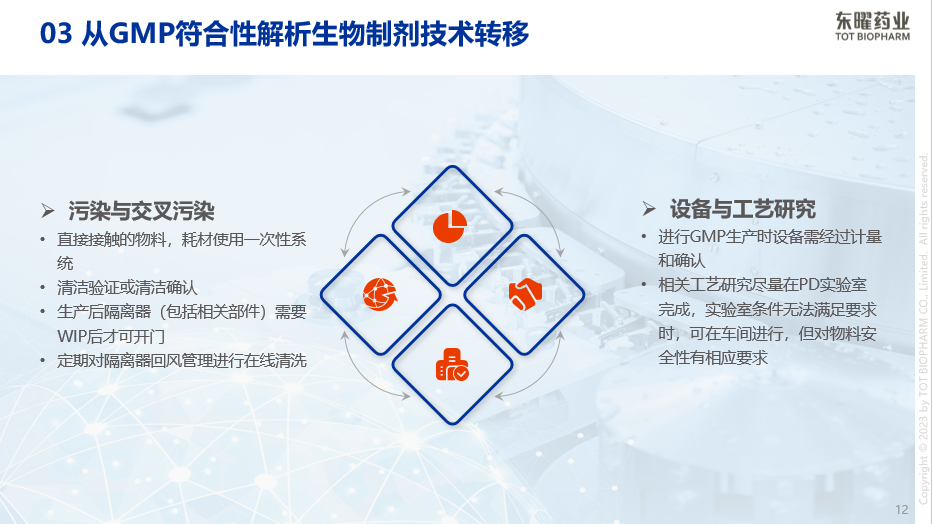
从GMP的方向切入,预防污染与交叉污染以及对设备与工艺的研究也是技术转移过程中不可或缺的细节。
针对生物制剂中的技术转移要点,周昀总监分享了一个实际案例:某双抗ADC项目为液体制剂,制剂处方开发均正常,未发现样品中有可见异物;在进行ENG run生产后对样品进行人工目检时发现约20%样品中有白色点状可见异物,通过对白色可见异物进行鉴定确定其成分,然后通过实验排除颗粒是在工艺过程中产生的,最终通过实验确认处方存在问题,需要重新开发。这一案例切实地阐明了在面对不同情况时应当如何分析,并制定相应的技术转移方案策略,最终成功地推进项目顺利落地。
东曜药业在生物药包括抗体、ADC领域深耕十余年,拥有药物开发全产业价值链经验,已建成符合GMP标准的集抗体、ADC原液及制剂于一体的商业化产线,配备国际一线品牌生产设备。抗体制剂线生产速度达18,000瓶/小时,年产量可达250批,ADC冻干制剂线每批冻干产能达5万瓶,年产能可达150批。东曜药业持续秉持“以品质 助创新 共成长”的服务理念,为产品高质量研发与商业化生产保驾护航,赋能合作伙伴,共创双赢。
关于东曜药业股份有限公司(股票代码:1875.HK)
东曜药业从事抗体及ADC药物开发10多年,具有丰富的工艺开发与商业化生产经验。
公司于2019年在香港联交所主板上市,2020年全面转型,致力于成为全球药物开发领域专业CDMO合作伙伴,提供生物药开发到生产一站式解决方案。
东曜药业拥有从研发、工艺开发、临床试验、注册报批到商业化生产的全流程经验,建立了完整的ADC技术平台,具备核心偶联工艺和放大的技术优势,以及ADC关键质量属性的自主分析能力,保证产品高质量开发。
在生产方面,东曜药业拥有多条集抗体、ADC原液(包含非毒偶联)及制剂于一体、国内产能领先的OEB-5级别ADC CDMO商业化生产线,避免了不同国家对于分段生产议题上可能的法规不确定性风险,抗体产能达万升级以上,并有商业化产品在线生产。
在质量体系方面,东曜药业质量管理体系满足中国/美国/欧盟申报要求,通过国家药品注册生产现场和GMP质量管理体系核查,具有丰富的产品上市注册核查经验,已为客户提供数百余个抗体及ADC项目的中美欧工艺开发、临床申报及生产服务。
东曜药业秉持“以品质 助创新 共成长”的服务理念,为产品高质量研发与商业化生产保驾护航,赋能合作伙伴,共创双赢。
往期推荐
业务垂询 bd@totbiopharm.com
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。