曜享干货 | 连接子(Linker)——mAb到ADC之路的关键
抗体偶联药物(ADC)是将具有靶向性的抗体和具有细胞毒活性的毒素小分子(payload)通过化学连接子(linker) 连接到一起组成的一个较为复杂的分子。近年来,人们对payload和linker的研究逐步深入,并且取得突破性进展。以Enhertu(DS-8201)为代表的ADC更是突破人们对传统ADC的理解,并大幅提高临床的治疗效果,成为重磅级的产品。近两年ADC药物也迎来了上市的爆发期,成为创新药领域最热门的赛道之一。
ADC的linker既要连接抗体和毒素,又需要在肿瘤细胞处可以裂解将毒素释放,这两个作用就决定了linker必须具备的两个特点: 第一,在体内循环系统里要稳定;第二,到达肿瘤细胞部位要能特异性释放活性成分。这样一对看似矛盾的需求就导致了linker的开发具有非常大的难度和挑战。
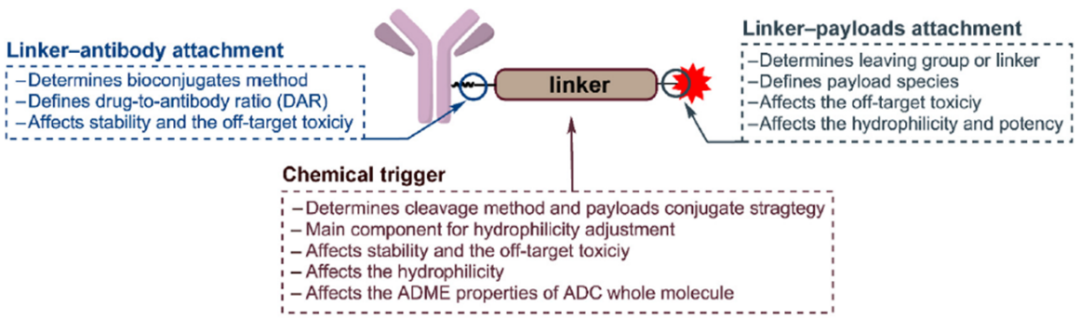
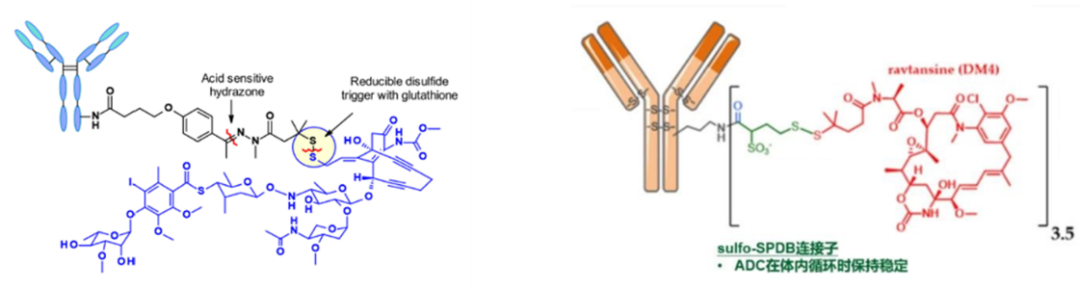
本文将分成三个方面介绍linker设计研究的进展,分别是触发linker断裂的化学基团、linker和抗体的连接位点以及linker和毒素的连接位点(图1)。
图1 触发linker断裂的化学基团、linker和抗体的连接位点以及linker和毒素的连接位点的作用[1]
1
触发Linker断裂的化学基团
因为是可以触发释放毒素的连接子,因此本文讲的都是可裂解连接子,不可裂解的连接子就不在此处介绍。可裂解连接子,顾名思义就是可以被裂解然后释放毒素的连接子。根据裂解机理的不同可以分为酶裂解连接子和化学裂解连接子。下面就为大家一一介绍这些连接子是如何设计并被触发从而释放毒素的。
1.1
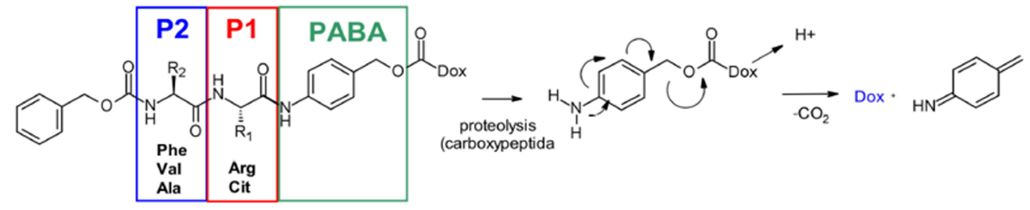
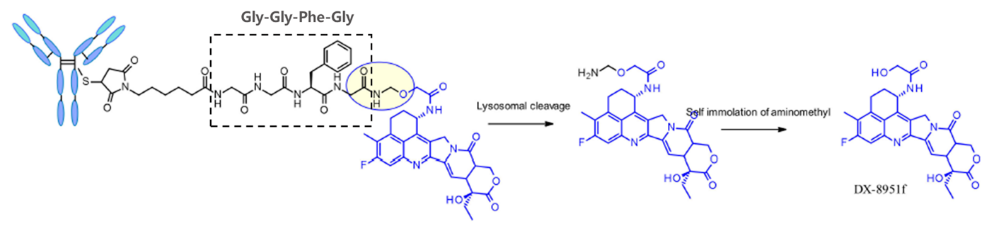
可以被组织蛋白酶裂解的linker。常见的是二肽(图2)或者四肽连接子(图3),这些肽段可以被多种组织蛋白酶裂解,然后裂解下来的部分发生自消除反应释放毒素。
图2 二肽连接子结构及其断裂释放毒素的机制[2]
图3 四肽连接子结构及其断裂释放毒素的机制[2]
1.2
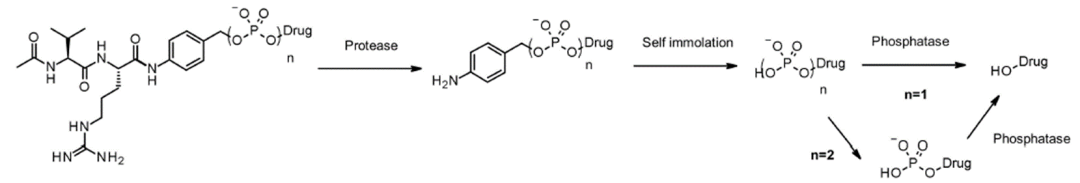
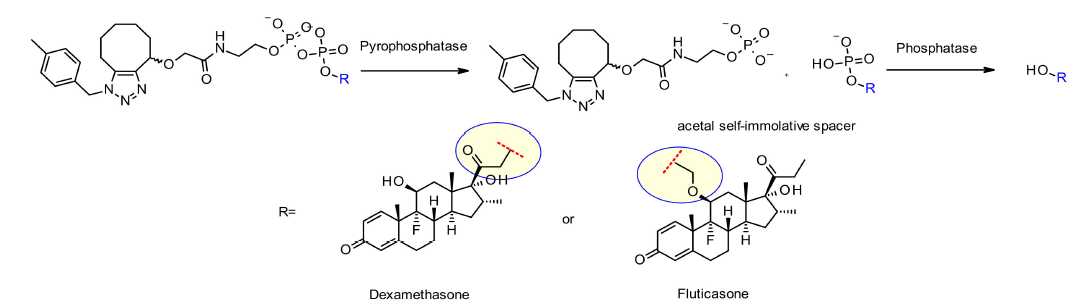
磷酸酶和焦磷酸酶裂解的linker。和组织蛋白酶一样,磷酸酶和焦磷酸酶也是一类在溶酶体中选择性表达的水解酶,针对这个特点就可以在linker的设计中加入磷酸基团或者焦磷酸基团,然后水解释放毒素(图4)。
图4 磷酸酶和焦磷酸酶裂解linker的结构及其释放机制[2]
1.3
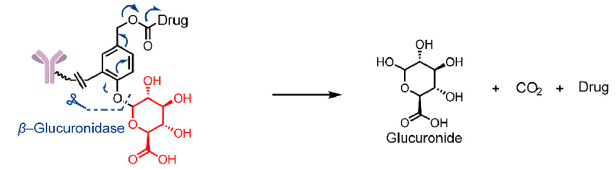
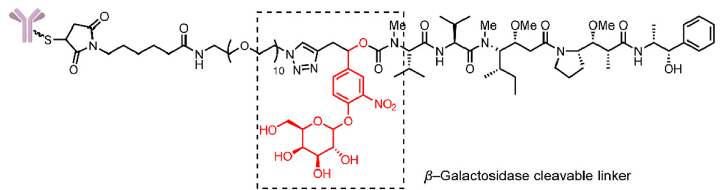
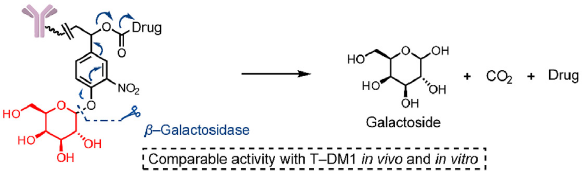
β-葡萄糖醛酸酶和β-半乳糖苷酶裂解的linker。此设计的linker中引入能被这两个酶特异性水解的基团+自降解spacer的组合,linker在β-葡萄糖醛酸和β-半乳糖基团被水解后经过自降解反应释放毒素(图5)。
图5 β-葡萄糖醛酸酶和β-半乳糖苷酶裂解linker的结构及其释放机制[1]
1.4
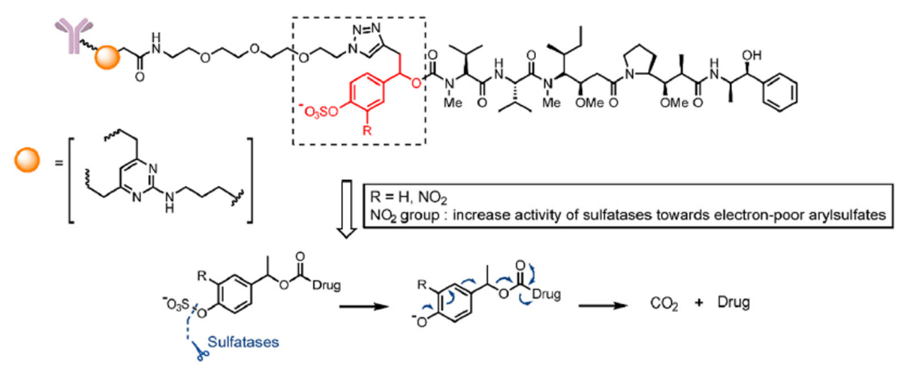
磺酸酯酶裂解的linker。和β-葡萄糖醛酸酶和β-半乳糖苷酶的设计思路一样,在linker中引入磺酸酯基团+自降解spacer的组合,linker被磺酸酯酶水解后经过自降解反应释放毒素(图6)。
图6 磺酸酯酶裂解linker的结构及其释放机制[1]
1.5
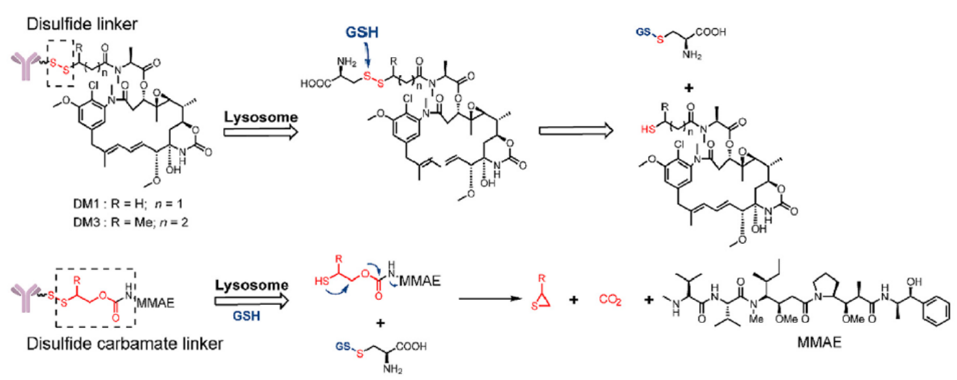
谷胱甘肽裂解的linker,也就是带有二硫键基团的linker。大部分肿瘤细胞中谷胱甘肽的含量都高于正常细胞,因其具有一定的还原性,可以还原二硫键从而释放毒素(图7)。
图7 谷胱甘肽裂解linker的结构及其释放机制[1]
1.6
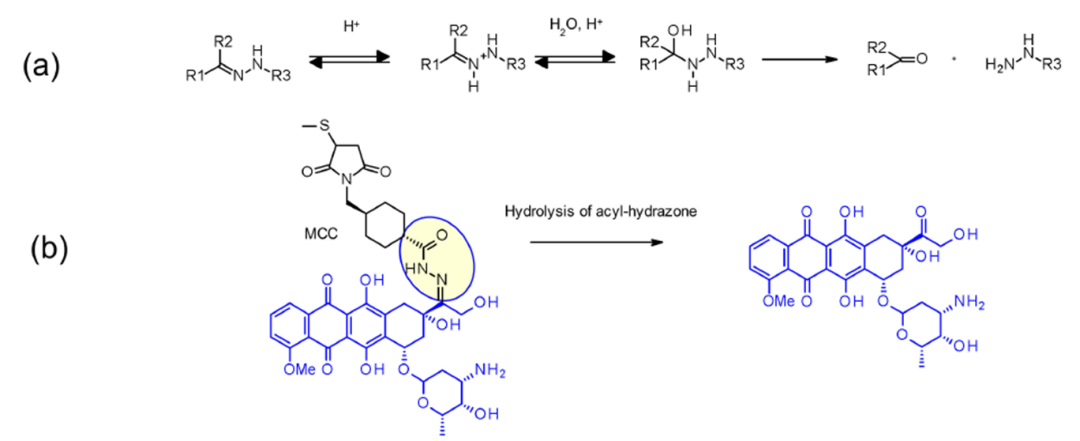
酸性条件下可以裂解的linker。相比正常体液和血液中中性偏碱的pH条件,肿瘤微环境的pH一般偏酸性,甚至可以低至6以下,这就可以设计对酸性条件敏感的linker基团,比如腙键和碳酸酯键等在中性条件稳定但酸性条件可以被裂解的基团(图8)。
图8 酸性条件下可以裂解linker的结构[1]
新的linker技术也在不断开发中,目前还有几类仍处于基础研究阶段尚未得到临床研究的认证,像是二价铁离子介导的芬顿反应裂解linker、光响应可裂解linker、生物正交可裂解linker等,此处不另做展开介绍。
2
Linker和抗体的连接位点
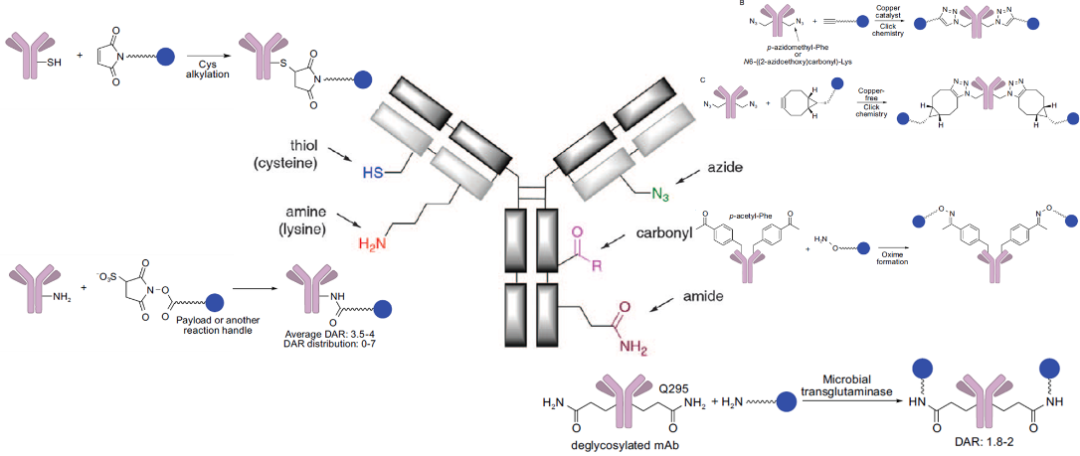
抗体分子中主要参与化学反应的基团是半胱氨酸的巯基和赖氨酸的伯氨基,参与了随机偶联ADC常用的两个反应,即巯基和马来酰亚胺的迈克尔加成反应、氨基的琥珀酰亚胺酯的取代反应。此外,可以在抗体中定点插入非天然氨基酸从而引入可反应的羰基和叠氮基,利用羰基和羟胺成肟反应以及叠氮基和炔基的click反应连上linker-drug,最后是抗体自带的谷氨酰胺,利用谷氨酰胺转移酶也可以实现偶联,这就涉及到酶催化的定点偶联(图9)。
图9 抗体中可以参与制备ADC的功能基团及其相应的反应方程式[3] [4]
此外,还有一个重要的连接位点就是抗体结构中的糖基化位点。抗体结构Fc结构域N297位是一个保守的糖基化位点,在该位点引入细胞毒素形成的糖链定点ADC化合物(glycosite-specific ADCs, gsADCs)具有不影响抗原结合、稳定性更好等优势,近年来受到广泛关注。
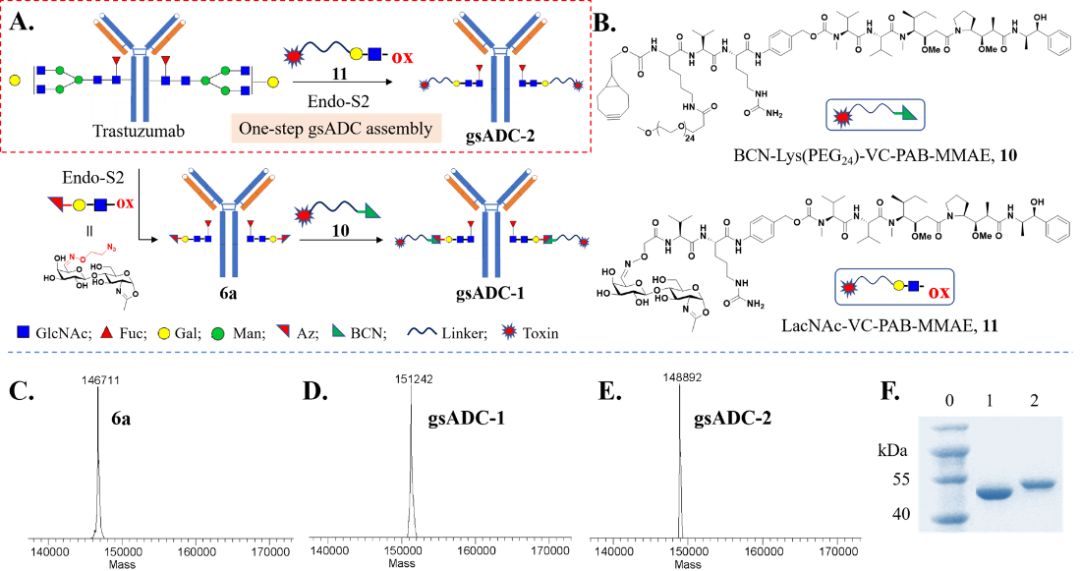
东曜药业和糖岭生物合作进行商业化开发和推广的DisacLinkTM技术也属于此类具有高度应用价值的定点偶联技术(图10),也是全球最先进的定点偶联技术之一,具有均一性高、工艺简洁、反应时间短、反应条件温和以及工艺综合成本低等显著特点。该类创新技术可以用于ADC新药的研发,衔接商业化应用,产生更加安全有效、患者可及度更高的新一代ADC产品,赋能ADC研发。
图10 DisacLinkTM糖定点偶联技术[5]
3
Linker和毒素的连接位点
3.1
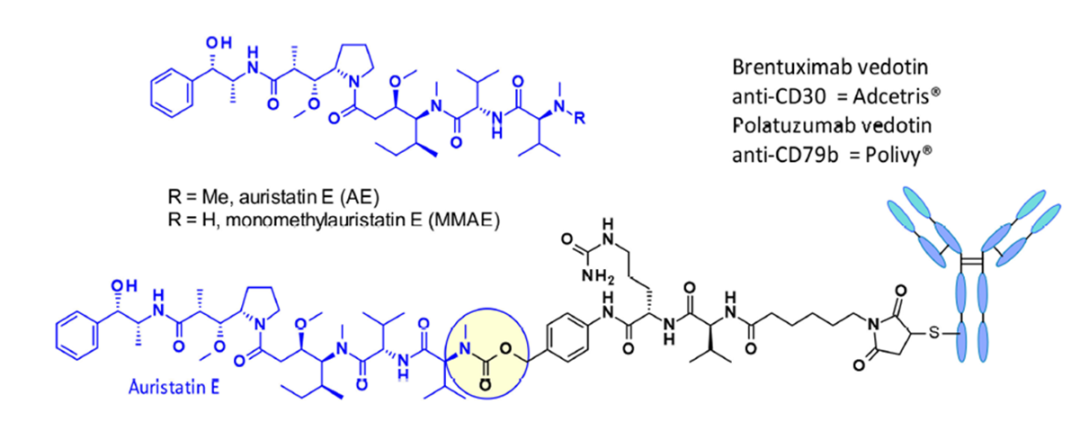
氨基甲酸酯键是目前使用最多的连接方式,payload中含有伯胺基和仲胺基的都可以采用这种连接方法,如上市ADC药物Adcetris和Polivy等即通过氨基甲酸酯键连接PAB和MMAE。
图11 氨基甲酸酯键连接位点结构[2]
3.2
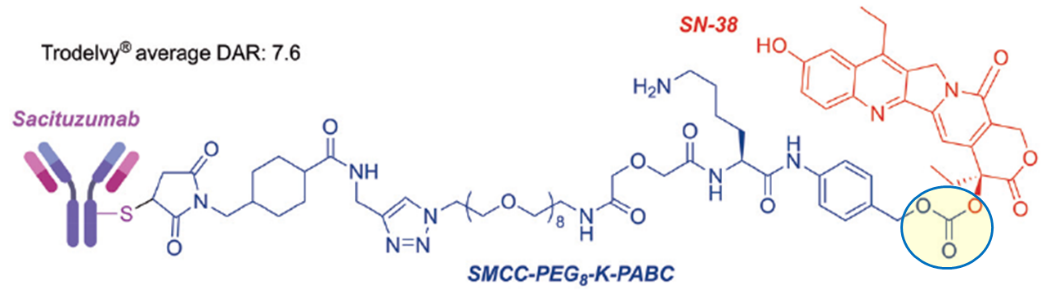
碳酸酯键:该linker和毒素连接位点同时是触发毒素释放的裂解基团,上市ADC药物Trodelvy采用的是此种连接方式(图12)。
图12 碳酸酯键连接位点结构[6]
3.3
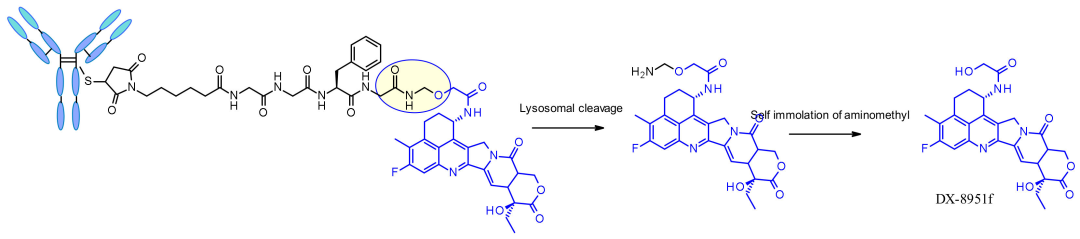
Enhertu的酰胺键连接位点有一个类似前药的设计,四肽连接子GGFG最后一个甘氨酸的羧基和氨基缩合成酰胺键,经酶切后氨基亚甲基自消除,最后释放出DXD(图13)。
图13 酰胺键连接位点结构[2]
3.4
另外还有两个典型的linker与毒素连接位点同样是裂解基团的设计。第一个是腙键连接位点,前文讲酸裂解linker的时候介绍过它是一个释放基团,同时也可以作为linker和payload连接位点使用(图14)。
图14 腙键接位点结构[2]
第二个是二硫键连接位点,前文讲谷胱甘肽裂解二硫键linker的时候介绍过它的释放机理,它同时具备连接毒素的作用,最早获批的ADC药物Mylotarg和最新获批的ADC药物Elahere就是采用二硫键连接和释放毒素(图15)。
图15 Mylotarg和Elahere的二硫键连接位点结构[2]
一个ADC的linker可以拆分成三个部分分别进行合理设计,以提高ADC药物在血液循环中的稳定性,并且使毒素能够在肿瘤细胞中特异性释放,从而达到在临床上扩大治疗窗口、增加疗效的目的,但好的linker的设计挑战也随之大大增加。一个linker就有如此多的设计和考量,再加上抗体、毒素以及偶联方式等不同选择,组合出种类繁多、各式各样的ADC候选分子,之后需要在这些候选分子中找到最优分子,这也是ADC药物开发难度大、开发风险高的原因所在。
凭借丰富实践经验、成熟技术平台及质量体系,东曜药业可为客户提供ADC一站式CDMO服务,服务范围涵盖研发到上市全流程,包含抗体/抗体中间体/ADC原液/ADC制剂的一地化开发与生产。目前为止,已有多个客户项目中美申报实绩。东曜药业秉承“以品质 助创新 共成长”的服务理念,与更多客户及合作伙伴携手助力ADC药物的研发、开发和生产,致力于成为行业领先、客户信赖的生物医药最佳合作伙伴。
参考文献
[1] Zheng Su, Dian Xiao, Fei Xie, Lianqi Liu, Yanming Wang, Shiyong Fan, Xinbo Zhou, Song Li, Antibody drug conjugates: Recent advances in linker chemistry[J], Acta Pharmaceutica Sinica B 2021;11(12):3889e3907.
[2] Vesela Kostova, Patrice Désos, Jérôme-Benoît Starck and Andras Kotschy, The Chemistry Behind ADCs[J], Pharmaceuticals, 2021, 14, 442.
[3] Floris L. van Delft and John M. Lambert, Chemical Linkers in Antibody–Drug Conjugates (ADCs)[M], The Royal Society of Chemistry 2022, Drug Discovery Series No. 81.
[4] Kyoji Tsuchikama, Zhiqiang An, Antibody-drug conjugates: recent advances in conjugation and linker chemistries[J], Protein & Cell, Volume 9, Issue 1, January 2018, Pages 33–46.
[5] Wei Shi, Wanzhen Li, Jianxin Zhang, Tiehai Li, Yakai Song, Yue Zeng, Qian Dong, Zeng Lin, Likun Gong, Shuquan Fan, Feng Tang, Wei Huang, One-step synthesis of site-specific antibodyedrug conjugates by reprograming IgG glycoengineering with LacNAc-based substrates[J], Acta Pharmaceutica Sinica B, 2022;12(5):2417-2428.
[6] Stephen J. Walsh, Jonathan D. Bargh, Friederike M. Dannheim, Abigail R. Hanby, Hikaru Seki, Andrew J. Counsell, Xiaoxu Ou, Elaine Fowler, Nicola Ashman, Yuri Takada, Albert Isidro-Llobet, Jeremy S. Parker, Jason S. Carroll and David R. Spring, Site-selective modification strategies in antibody–drug conjugates[J], Chem. Soc. Rev., 2021,50, 1305.
关于东曜药业股份有限公司(股票代码:1875.HK)
东曜药业从事抗体及ADC药物开发10多年,具有丰富的工艺开发与商业化生产经验。
公司于2019年在香港联交所主板上市,2021年全面转型,致力于成为全球药物开发领域专业CDMO合作伙伴,提供生物药开发到生产一站式解决方案。
东曜药业拥有从研发、工艺开发、临床试验、注册报批到商业化生产的全流程经验,建立了完整的ADC技术平台,具备核心偶联工艺和放大的技术优势,以及ADC关键质量属性的自主分析能力,保证产品高质量开发。
在生产方面,东曜药业拥有多条符合GMP标准的集抗体、ADC原液及制剂于一体、国内产能领先的OEB-5级别ADC CDMO商业化生产线,避免了中国与其他国家对于分段生产议题上的法规不确定性风险,抗体产能达万升级以上,并有商业化产品在线生产。
在质量体系方面,东曜药业质量管理体系满足中国/美国/欧盟申报要求,通过国家药品注册生产现场和GMP质量管理体系核查,具有丰富的产品上市注册核查经验,已为客户提供数十个抗体及ADC项目的中美欧工艺开发、临床申报及生产服务。
东曜药业秉持“以品质 助创新 共成长”的服务理念,为产品高质量研发与商业化生产保驾护航,赋能合作伙伴,共创双赢。
业务垂询 bd@totbiopharm.com
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。