曜享干货 | 创新药国内通用名申请之路 (三)国内通用名申请
创新药国内通用名申请,通常需要经过三个阶段:1)CAS号申请;2)INN申请;3)通用名申请。之前曜享干货已经介绍前两个阶段CAS号申请和INN申请 ,本期给大家带来的是第三阶段——通用名申请。
药品通用名的定义及组成
中国药品通用名称(China Approved Drug Names, 简称:CADN):列入国家药品标准(中国药典、局颁标准)和药品注册标准的药品名称,是药品的法定名称。药品通用名反映不同药品之间区别,由药品管理的专门机构规定,具有强制性和约束性,属于公有领域的名称。
药品的英文名应尽量采用世界卫生组织编订的国际非专利药名(International Nonproprietary Names for Pharmaceutical Substances,简称INN);没有INN可采用其他合适的英文名称。
1
化学药通用名命名
原料药:中文通用名尽量与英文名相对应。可采取音译、意译或音、意合译,一般以音译为主。命名细则详见《中国药品通用名称命名原则》。
制剂:原料药名称列前,剂型名列后。药品制剂名称中说明用途或特点等的形容词宜列于药名之前。复方制剂根据处方组成的不同情况可采用不同的方法命名,详见《中国药品通用名称命名原则》。
2
生物制品通用名命名
根据中国药典2020年版三部《生物制品通用名称命名原则》,治疗性重组蛋白(多肽)类、基因治疗和细胞治疗类生物制品,原则上应采用世界卫生组织国际非专利名称(WHO INN),其通用名称命名应符合以下基本原则:
1)采用INN 命名的生物制品,其通用名称应符合INN 命名原则,中文通用名称原则上应与其英文INN 相对应,可采用音译、意译或音意合译的方式,并结合具体剂型进行命名。
2)生物制品中文INN应在读音和撰写方面具有唯一性,不应和常用的名称相混淆。
3)生物制品中文INN 应尽可能保留所含相关英文词干(包括中间词干和后缀)的音译、意译或音意合译含义。
中国药典2020年版三部《生物制品通用名称命名原则》之前主要依据《中国药品通用名称命名原则》(2006年颁布),其规定,已有 INN 名称的生物制品中文通用名称应尽量与其英文名相对应,其中文名应以意译为主,亦可音译或音、意合译;尚无 INN 名称的,可以疾病、微生物、特定组成成分或材料等命名,并应标明药品剂型。
药品通用名与商品名/商标的区别
药品商品名:申请人为方便其药品上市销售而申请的、国家药品监督管理部门批准的药品名称,是特定企业使用的专用名称,经过注册,具有专用权。药品商品名称仅限于符合新药要求的化学药品、生物制品(含生物类似药)及境外生产中药可以申请使用。
药品商标:市场上具有相同通用名称的药品可能有多个上市许可持有人,为了市场竞争和知识产权保护的需要,持有人往往给自己生产的药品注册商标,以示区别。所有类型药品都可以注册商标并使用。
综上,对于创新药而言,其可以同时具有通用名、商品名和商标。那三者之间有什么关系呢?
①使用强制性:仅药品通用名需强制使用,商品名和商标非强制。
②使用范围及通用性:通用名针对相同成分相同剂型相同给药途径的同类药品,是这类药品的统一名称;商品名针对某一创新药(含生物类似药)及境外生产中药,是该药品的专有名称;商标针对所有类型的每一个药品,是该药品的专有标识。仿制药只允许有商标但不得使用商品名(现法规前已获得商品名的仿制药除外)
③核准机构:通用名由药典委员会负责组织制定并报国家药品监管管理局备案;商品名由国家药品监督管理局核准,且前提需经商标注册;商标由国家知识产权局商标局核可。
通用名与INN的关系
《中国药品通用名称命名原则》的总则第5条:“药品的英文名应尽量采用WHO组织编订的INN”。
中国药典2020年版三部《生物制品通用名称命名原则》提到:“治疗性重组蛋白(多肤)类、基因治疗和细胞治疗类生物制品,原则上应采用世界卫生组织(World Health Organization , WHO)国际非专利名称(International Nonproprietary Name, INN)”。
上述两命名原则均要求:采用INN 命名的药品/生物制品,中文通用名原则上应与其英文INN 相对应。
当药品或生物制品获得INN之后,中国国家药典委员会根据WHO公布的INN名单,不定期组织开展INN名称相应中文名称的审核工作,并在药典委的网站上公示。
因此,对于在中国申请上市的药品,一般采用INN作为药品的英文名,对应的中文通用名则可按照命名原则拟定(中国药典委公示的名称或企业自行拟定),且需在提交药品上市申请时经药典委核可(创新药、生物类似药及境外中药)并最终由NMPA确认。
需通用名申请的情形
1)申报药品拟使用的药品通用名称,未列入国家药品标准或者药品注册标准的,申请人应当在提出药品上市许可申请时同时提出通用名称核准申请。
2)对于已有通用名称的药品,药品审评中心在上市申请的审评过程中认为需要核准药品通用名称的。
注:创新药通常都需要申请通用名称。
通用名申请
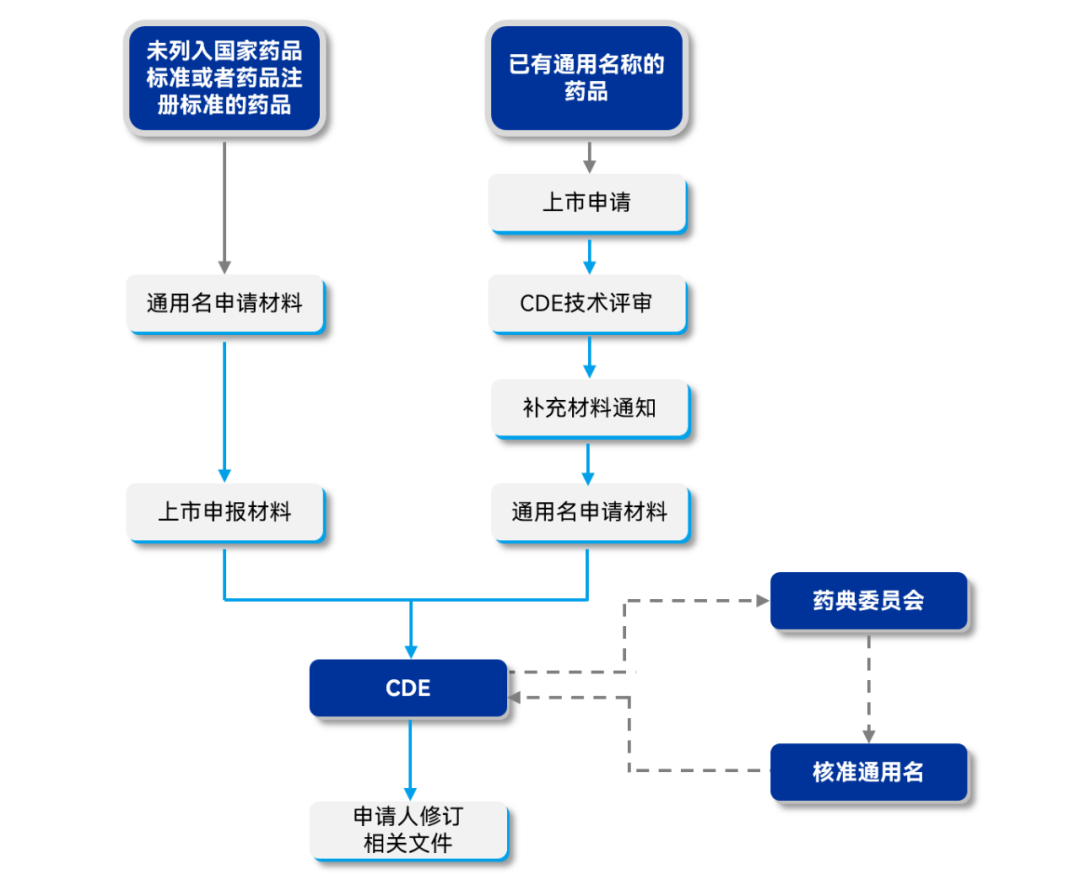
简要流程图:
申请准备
未列入国家药品标准或者药品注册标准的药品,如已取得INN英文名称、且药典委已发布了相应的INN中文名称,则可使用该INN中文名称并结合剂型按照通用名命名原则申请中国药品通用名(CAND)并准备相关证明文件。若无INN英文名或已有INN英文名但药典委员会尚未发布相对应的INN中文名称,则可按照通用名称命名原则并结合剂型,准备几个中文通用名(五个以内)并说明理由,制作通用名申请资料。
对于已有通用名的药品,如接到药品审评中心的通知要求重新核准药品通用名,也需参照上述要求准备通用名及申请资料。
注:自2023年1月1日起已采用电子形式提交申报资料,除完整的申报资料或补充资料光盘外,通用名称核准资料需另外再单独准备1套光盘。
申请提交
在创新药提交上市申请时,将通用名申请材料整合入CTD申报资料模块一“1.3.5药品通用名称核准申请材料”项下,随药品上市申请一并提交。
若是接到药品审评中心的通知要求重新核准药品通用名称,一般与其他补充资料一并提交至药审中心。
通用名核准
上市申请被受理后或审评中心接到发补资料后,药审中心将通用名称核准申请材料转交给药典委;药典委在收到材料后先进行完整性审核,审核通过后进行登记,分派给相关业务处室对通用名称进行核准。复核通过的通用名由分管秘书长签发。自登记时间至签发日期的工作时限为30个工作日。
通用名发放
药典委将通用名核准结果发送药审中心,并抄送申请人。
相关文件修订
产品批准上市前,申请人接药审中心的通知后对批准文件及相关附件中的通用名进行修订。
通用名申请过程中的沟通交流
药典委对通用名申请材料进行审核,如需申请人进一步提供相关资料、或相关问题可能对申请方造成影响时,药典委将联系申请人。
如申请人对核准名称存在异议时,也可联系药典委。如有必要,由药典委组织申请人、审评专家、相关单位或部门召开专家讨论会,确定最终意见。
至此,我们完整分享了创新药国内通用名申请三部曲,希望对大家的工作有所帮助, 后续我们将持续分享其他实用的经验知识,敬请期待!
东曜药业在苏州总部和北京设有注册事务处,拥有人员稳定且具备丰富注册申报实战经验的团队,熟知各监管机构的法律法规及沟通机制。能够为客户提供搭配产品研发、申报上市及上市后管理的产品生命周期中全方位的法规支持CDMO服务,包括法规策略咨询、注册策略/申报方案制定、项目申报风险评估、药学相关申报资料及非临床资料撰写等服务。目前已完成超过10个境内外注册申报项目,包括中美IND申报、ANDA/NDA申报。
联系信息:
邮箱: TOT-RA@totbiopharm.com
关于东曜药业股份有限公司(股票代码:1875.HK)
东曜药业从事抗体及ADC药物开发10多年,具有丰富的工艺开发与商业化生产经验。
公司于2019年在香港联交所主板上市,2021年全面转型,致力于成为全球药物开发领域专业CDMO合作伙伴,提供生物药开发到生产一站式解决方案。
东曜药业拥有从研发、工艺开发、临床试验、注册报批到商业化生产的全流程经验,建立了完整的ADC技术平台,具备核心偶联工艺和放大的技术优势,以及ADC关键质量属性的自主分析能力,保证产品高质量开发。
在生产方面,东曜药业拥有多条符合GMP标准的集抗体、ADC原液及制剂于一体、国内产能领先的OEB-5级别ADC CDMO商业化生产线,避免了中国与其他国家对于分段生产议题上的法规不确定性风险,抗体产能达万升级以上,并有商业化产品在线生产。
在质量体系方面,东曜药业质量管理体系满足中国/美国/欧盟申报要求,通过国家药品注册生产现场和GMP质量管理体系核查,具有丰富的产品上市注册核查经验,已为客户提供数十个抗体及ADC项目的中美欧工艺开发、临床申报及生产服务。
东曜药业秉持“以品质 助创新 共成长”的服务理念,为产品高质量研发与商业化生产保驾护航,赋能合作伙伴,共创双赢。
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。