摆脱胰岛素?糖尿病干细胞疗法机遇与挑战并存
最新流调数据显示,目前我国糖尿病患病率为11.2%,以2型糖尿病为主。相比起2型糖尿病患者,1型糖尿病主要发病于青少年群体,目前我国青少年儿童糖尿病的患病人数排全球第4,并且每年约有1.3万人被新确诊。
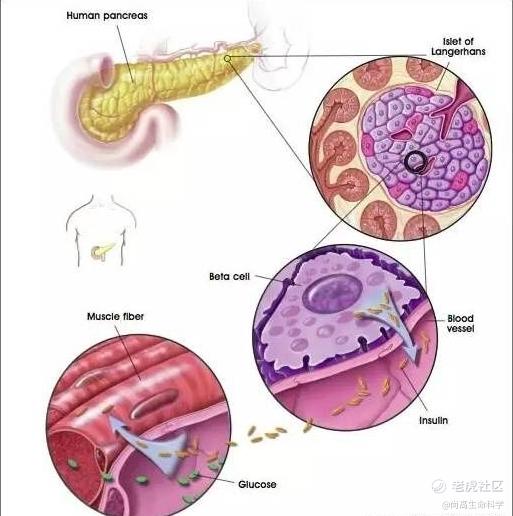
1型糖尿病(T1D)最明显的特点为早发,一般在儿童或青少年时期就已经发病。目前,糖尿病治疗的主要手段是注射胰岛素并配合血糖监控。然而,传统的胰岛素补充并不能实现根本性的治疗,并且对糖尿病并发症的控制力也不足,存在高度未满足的医疗需求。
胰岛β细胞衰竭和胰岛素抵抗是导致2型糖尿病发展的主要机制。目前干预2型糖尿病的传统方法是药物和胰腺移植,但抗糖尿病药只能暂时缓解症状,不能从根本上改善疾病。因此,人们正在关注寻找合适的胰岛细胞再生和修复方法。
干细胞疗法成为糖尿病热门研究
而干细胞是一类具有强大的自我复制能力的多潜能细胞,其在一定条件下分化为各种细胞、组织、器官的功能,并且细胞来源丰富、免疫原性低。因此,可以通过体内外诱导干细胞定向分化成为具有分泌胰岛素能力的细胞,以恢复胰岛功能,从而达到有效干预糖尿病的目的。
我国学者在干细胞治疗糖尿病的基础和临床研究方面做出了突出贡献,经过科学家的不懈努力,干细胞治疗糖尿病不断传来突破。以下是干细胞移植干预糖尿病四种作用机制:
1.干细胞是一种多能性的、自我更新的、对免疫反应的调节能力强的细胞,它可以诱导分化为胰岛素分泌细胞(insulin-producing cells,IPCs),以促进胰腺再生和减轻胰岛素抵抗,并为糖尿病干预的胰岛细胞移植提供替代选择。
2.干细胞除了能够分化为IPC外,还可以迁移到受损的胰岛细胞,分泌多种细胞因子和生长因子,并自分泌活性,从而促进胰岛β细胞的再生。
3.干细胞具有免疫原性低、免疫调节性差等特点,可保护胰岛β细胞,减少自体免疫所致损伤。
4.干细胞通过激活胰岛素受体底物信号通路,使胰岛素抵抗在周围胰岛素靶区得到缓解,从而达到稳定血糖的目的,有效预防糖尿病并发症。
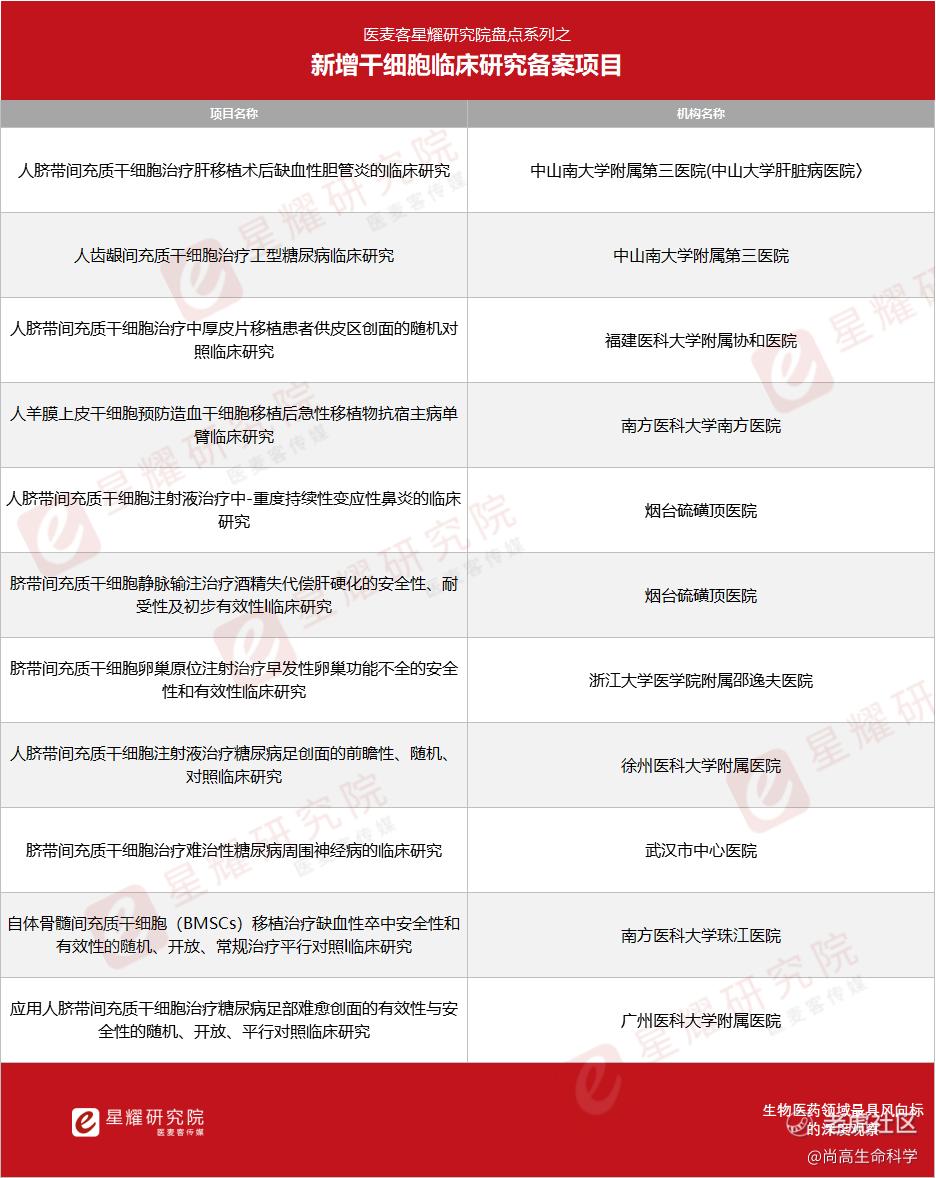
日前,中国医药生物技术协会公布了最新完成备案的2家干细胞临床研究机构和11个干细胞临床研究项目。至此,我国有60余个干细胞临床研究项目已经完成备案,其中就包括了干细胞疗法干预糖尿病的相关项目。
从统计的数据可知,在新增的11个干细胞临床研究备案项目中,有4个与糖尿病相关,是干细胞临床研究的热门领域。
干细胞移植治疗糖尿病方法
自体外周血干细胞移植
在临床上根据自体干细胞采集的方法不同分为自体骨髓干细胞移植和自体外周血干细胞移植。通过药物动员骨髓在较短时间在外周血中收集到尽可能多的造血干细胞(HSC),利用HSC有重建造血、免疫系统的功能,重建Ⅰ型糖尿病患者自身免疫系统,从而摆脱胰岛素。
骨髓干细胞移植
间充质干细胞(MSC)具有极强的自我更新能力与多向分化潜能,在胰腺微环境下可分化。
为胰岛素分泌细胞,并促进内源性胰岛细胞的再生,从而重建胰岛功能,同时诱导免疫调控,阻止进一步免疫破坏,协助患者重建正常的免疫系统,达到从源头上根治糖尿病的目的。
由于外周血中MSC含量较少,大量MSC存在骨髓中。自体间充质干细胞(MSC)治疗糖尿病,是通过骨髓获得足够量的MSC,回输给患者达到根治糖尿病的目的。
干细胞治疗糖尿病的临床案例
1.国家干细胞工程研究中心研究组对10例Ⅱ型糖尿病患者输注间充质干细胞,每隔1个月输注1次,连续3次,发现日胰岛素总量从63.7U减少为34.7U,空腹C肽水平从4.1ng/mL上升至5.6ng/mL,取得良好的效果。
2.我国学者对13例Ⅰ型糖尿病患者进行干细胞移植,移植后胰岛素用量明显减少且血糖控制达标,其中2例患者停用胰岛素时间分别为3年和4年。研究人员认为这是干细胞通过调节免疫活性细胞改善胰岛β细胞功能而实现。
3.广州某医院研究组使用脐带间充质干细胞治疗22例Ⅱ型糖尿病患者,结果显示患者HbA1c从基线的8.2%下降至3月后的6.89%,随访至12月时仍稳定在7.0%;空腹C肽升高,CD3+T淋巴细胞的数量下降。
小结
目前干细胞领域飞速发展,各项技术正处在突破性发展阶段,同时也面临诸多挑战:干细胞来源广泛,但细胞制备标准和评价体系有待进一步统一。无论是干细胞治疗的有效性和安全性,还是治疗时机、长期疗效、适应人群等方面问题,均尚未得到很好的解决,行业内监管机制尚不健全。
相信不久的将来,在领域内专家学者和监管机构的共同努力下,一定可以攻坚克难,使干细胞治疗在糖尿病领域大有所为。
来源:医麦客
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。