迈威生物-B(688062),递交招股书,拟赴香港上市 | 医疗健康企业.IPO上市
2026年3月25日,来自上海的A股上市公司迈威(上海)生物科技股份有限公司 Mabwell (Shanghai) Bioscience Co., Ltd. (下称"迈威生物”)向港交所递交招股书,拟香港主板挂牌上市。这是继其于2025年1月6日、2025年8月29日先后两次递表失效后的再一次申请。
迈威生物,此前收到中国证监会境外发行上市备案通知书,可发行不超过6266.46万股境外上市普通股并在香港联合交易所上市。
迈威生物(688062.SH),于2022年1月18日在A股上市,截至2026年3月25日收市,总市值约人民币131亿元。
迈威生物招股书链接:
https://www1.hkexnews.hk/app/sehk/2026/108329/documents/sehk26032501611_c.pdf
主要业务
迈威生物,成立于2017年,作为一家以药物研发方面的创新能力以及从药物发现至商业化销售的端到端能力而闻名的中国制药公司,主要专注于自主开发肿瘤和年龄相关疾病药物,涉及肿瘤、免疫、眼科、骨科等领域。
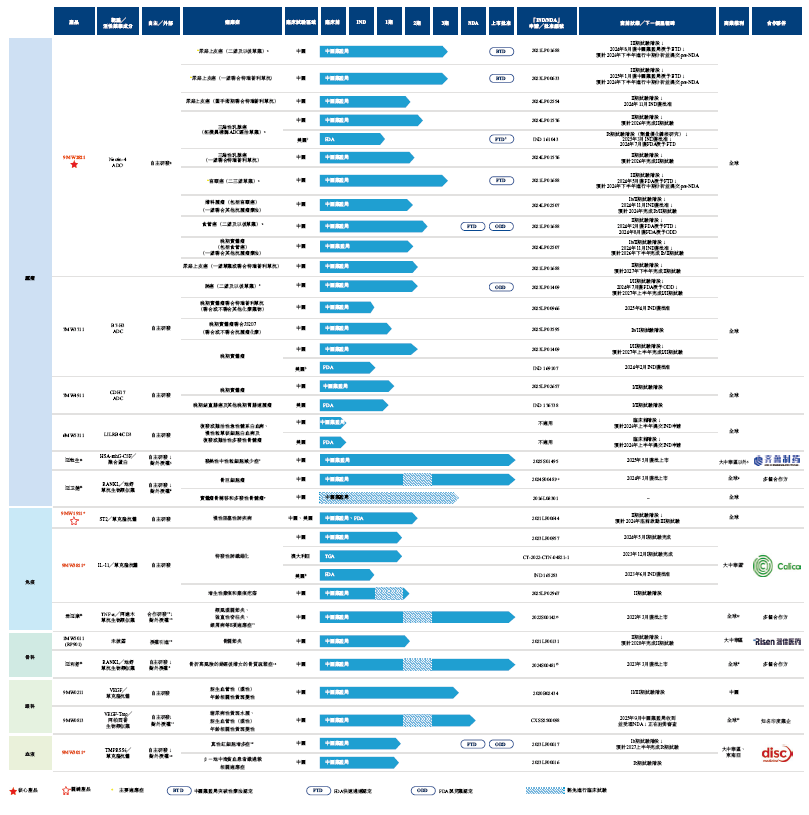
迈威生物,建立的管线产品组合,包括10个以上不同品种的药物资产,包括:
抗体偶联药物ADC
核心产品9MW2821(bulumtatug fuvedotin(BFv),靶向Nectin-4的ADC候选药物)。目前,就临床开发阶段而言,9MW2821是在中国开发的用于治疗尿路上皮癌的所有靶向Nectin-4 ADC中进展最快的,仅次于Padcev。9MW2821也是全球首款进入宫颈癌关键III期试验阶段的靶向Nectin-4 ADC。公司正在进行9MW2821的多项临床试验,其中包括(i) 9MW2821治疗尿路上皮癌的III期试验,(ii) 9MW2821治疗宫颈癌的III期试验,(iii) 9MW2821治疗三阴性乳腺癌的II期试验;及(iv) 9MW2821治疗晚期食管癌的II期临床试验;
7MW3711(靶向B7-H3ADC),分别于2023年8月和2023年9月在中国启动两项I/II期临床试验,以评估7MW3711单药治疗晚期实体瘤的安全性和有效性。此外,于2024年7月,FDA批准了用于治疗小细胞肺癌的ODD。于2025年4月,国家药监局批准公司提交的7MW3711联合特瑞普利单抗(联合或不联合其他化疗药物)治疗晚期实体瘤受试者的Ib/II期联合疗法临床试验的IND申请。于2026年2月,公司启动7MW3711联合JS207或JS207及抗肿瘤疗法治疗晚期实体瘤患者的Ib/II期临床试验。
7MW4911(靶向CDH17 ADC),2025年8月,FDA受理公司开展7MW4911的I/II期临床试验的IND申请。2025年10月,7MW4911获国家药监局IND批准。2025年11月,公司启动针对晚期实体瘤患者的I期临床试验。2026年1月,公司在美国启动7MW4911的临床试验。
其他差异化模态药物
9MW3811(一款用于纤维化相关疾病及癌症治疗的靶向IL-11的人源化单抗),分别于2023年12月及2024年5月在澳大利亚及中国完成9MW3811针对健康受试者的I期临床试验。此外,公司于2023年6月就针对特发性肺纤维化的临床试验获得FDA的IND批准。公司于2025年8月向国家药监局提交9MW3811针对病理性瘢痕(包括增生性瘢痕和瘢痕疙瘩)临床试验的IND申请,国家药监局于2025年11月授予IND批准,使9MW3811成为首款进入病理性瘢痕(包括增生性瘢痕和瘢痕疙瘩)治疗临床阶段的IL-11靶向药物。公司于2025年12月启动9MW3811针对病理性瘢痕(包括增生性瘢痕和瘢痕疙瘩)的临床试验。
关键产品9MW1911(中国首个获批进行临床开发靶向ST2的自主开发候选药物),于2023年7月在中国启动针对COPD患者的Ib/IIa期试验,预期于2026年上半年完成该试验。于2025年7月在中国启动针对COPD患者的另一项II期试验,预期于取得至少120名受试者的52周随访数据后进行中期分析,并于2027年下半年完成所有患者随访。公司计划于2026年下半年推进在中国进行的9MW1911治疗COPD患者的III期临床试验。2025年12月,FDA授予在美国开展9MW1911治疗COPD的IIa期临床试验的IND批准。
9MW3011(一款重组人源化抗TMPRSS6单抗,为全球开发状态领先的靶向TMPRSS6治疗药物),于2024年5月在中国完成针对健康受试者的I期试验。此外,公司计划于2027年上半年在中国完成针对真性红细胞增多症患者的两项Ib期临床试验。
1MW5011(RP901)(一款用于骨关节炎治疗的小分子药物),用于治疗膝骨关节炎的II期临床试验正在进行患者招募,预计该试验将于2028年完成。此外,公司于2025年12月启动治疗膝骨关节炎患者的Ib期试验。
9MW0211(一款重组人源化单克隆抗体,靶向VEGF-A),于2019年5月完成治疗眼科疾病的I期试验。I期试验结果表明9MW0211具有良好的安全性及疗效。公司于2021年5月在中国启动II/III期临床试验,于2025年12月完成该试验,并计划于适当时候向国家药监局提交NDA。
9MW0813(一款重组人VEGF受体- 抗体融合蛋白阿柏西普的生物类似药),于2024年12月完成9MW0813的III期临床试验,并已向国家药监局提交NDA,NDA已于2025年9月获受理。
已上市药物
迈威生物的四款产品君迈康®、迈卫健®(肿瘤)、迈利舒®(骨科)、迈粒生®(发热性中性粒细胞减少症)已成功上市。
迈威生物的收入来自药品销售、对外授权收入。
股东架构
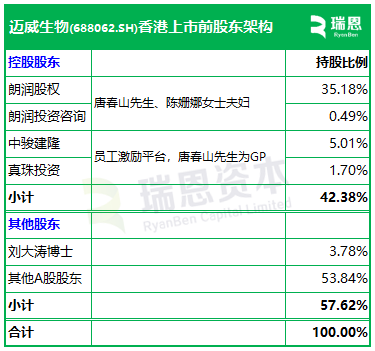
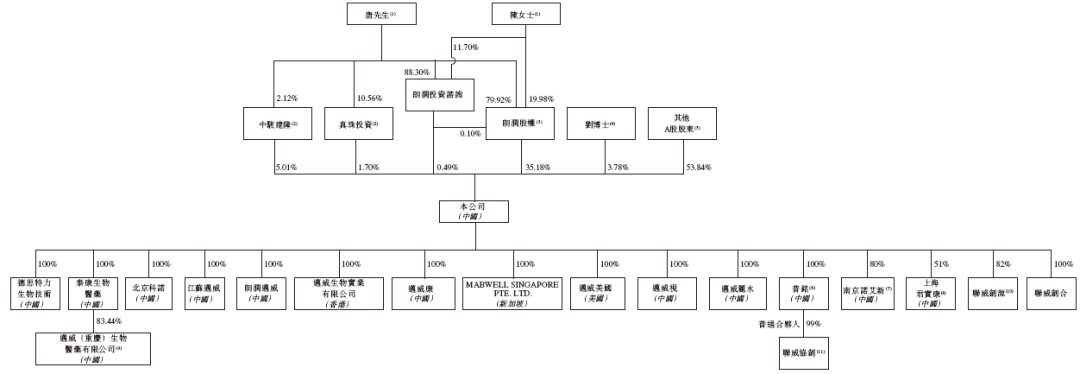
招股书显示,迈威生物在上市前的股东架构中,
唐春山先生、陈姗娜女士夫妇分别通过朗润股权、朗润投资咨询、中骏建隆(员工激励平台,唐先生为GP)、真珠投资(员工激励平台,唐先生为GP),分别持股35.18%、0.49%、5.01%、1.74%,合共持股约42.38%。
刘大涛博士,持股3.78%;
其他A股股东,持股53.84%。
董事高管
迈威生物董事会由10名董事组成,包括:
-
5名执行董事:
唐春山先生(控股股东);
刘大涛博士(董事长、总经理);
武海博士(副总经理兼研发总裁);
胡会国先生(副总经理兼董事会秘书);
桂勋博士(职工代表董事,副总经理);
-
1名非执行董事:
吴玉锋先生(海南拾玉私募管理合伙人);
-
4名独立非执行董事:
秦正余先生(紫江企业(600210.SH)首席财务官、副总经理);
许青博士(中国医药生物技术协会副理事长);
赵倩博士(上海交通大学医学院教授);
王芳女士(衡宽国际集团执行董事)。
除执行董事外,高管包括:
王树海博士(副总经理);
李瀚先生(副总经理);
倪华先生(副总经理);
陈曦女士(副总经理);
华俊先生(副总经理、财务负责人)。
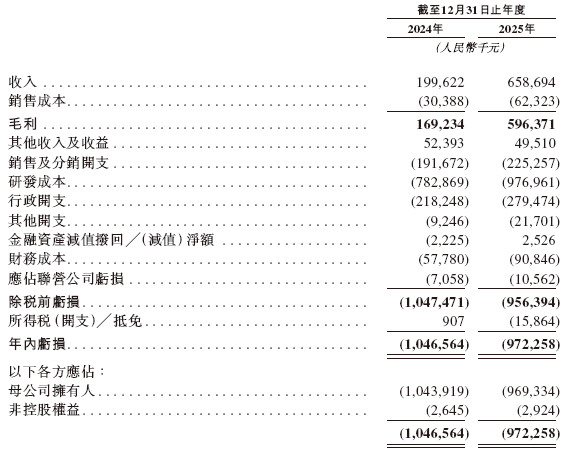
公司业绩
招股书显示,在过去的2024年和2025年,迈威生物的营业收入分别为人民币2.00亿和6.59亿元,相应的研发开支为人民币7.83亿和9.77亿元,相应的净亏损分别为人民币10.47亿和9.72亿元。
中介团队
迈威生物是次IPO的中介团队主要有:
中信证券、海通国际为其联席保荐人;
安永为其审计师;
竞天公诚为其公司中国律师;
达维为其公司香港及美国律师;
金杜为其券商中国律师;
史密夫斐尔为其券商香港及美国律师;
新百利融资为其合规顾问;
弗若斯特沙利文为其行业顾问。
*疏漏难免,敬请指正
版权声明:“瑞恩IPO上市”主要跟踪关注香港上市、澳门上市、美国上市等,所有原创文章,转载须联系授权,并在文首/文末注明来源、作者、微信ID,否则我们将向其追究法律责任。部分文章推送时未能与原作者或公众号平台取得联系。若涉及版权问题,敬请原作者联系我们。
更多香港IPO、美国IPO等境外上市资讯,敬请浏览:www.hkmipo.com
相关阅读
北京企业香港上市:2025年以来上市17家,目前正在申请的至少46家
上海企业香港上市:2025年以来上市24家,目前正在排队申请的至少58家
广东企业香港上市:2025年以来上市22家,即将上市2家,目前正在排队申请的至少117家
浙江企业香港上市:2025年以来上市15家、募资316亿,目前正在申请的至少60家
江苏企业香港上市:2025年以来上市18家、募资320亿,目前正在申请的至少55家
福建企业香港上市:2025年以来11家香港上市,目前至少13家正在排队
山东企业香港上市:2025年以来5家香港上市,目前至少26家正在排队
安徽企业香港上市:2025年以来上市3家、募资110亿,目前正在申请的至少18家
免责声明:上述内容仅代表发帖人个人观点,不构成本平台的任何投资建议。