本文转自微信公众号“汉靓的医药科技前沿”。
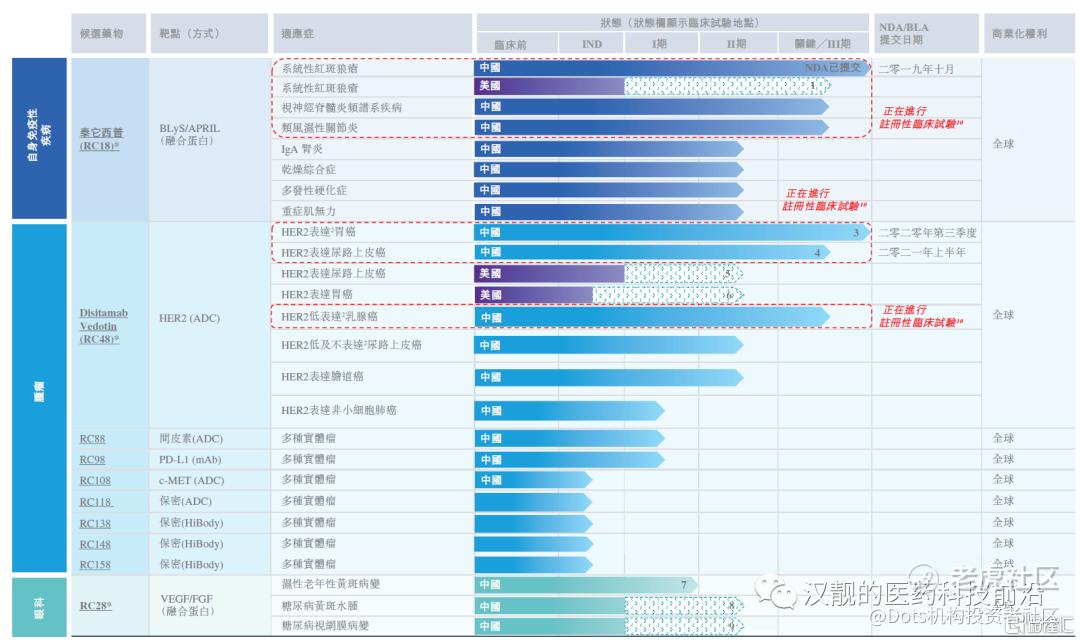
最近的香港生物科技板也可以说是异常热闹,多家生物医药公司陆续递交招股书,例如$荣昌生物-B(09995)$、药明巨诺,和铂医药、德琪医药等。本期我们把目光投向荣昌生物,从其最新的研发管线(图1)可以看到,已有五款药物进入临床阶段,核心产品包括已在系统性红斑狼疮(Systemic Lupus Erythematosus,以下简称SLE)领域递交NDA的泰它西普(Telitacicept;RC18);完成注册性临床、靶向Her2的ADC药品Disitamab vedotin(RC48),以及靶向VEGF和FGF的融合蛋白RC28。本期将和大家介绍泰它西普、已获批上市的贝利尤单抗,以及其它生物制剂在SLE领域的最新进展。
本期的节目分为三个部分:1)泰它西普的详细介绍;2)贝利尤单抗的详细介绍;3)具有代表性的生物制剂在SLE领域的进展。
图1:荣昌生物的产品管线
资料来源:荣昌的招股书
第一部分:荣昌生物的核心产品泰它西普的原理和临床数据
1.1 泰它西普的原理
泰它西普是一款重组融合蛋白(TACI-Fc),同时靶向两个重要的细胞因子:B淋巴细胞刺激因子(BLyS)和增值诱导配体(APRIL),其中,BLyS和APRIL对于B细胞的成熟和发育成浆细胞都起到重要作用,且在若干条件下共同刺激T细胞,所以BLyS和APRIL都成为了自体免疫领域的重要靶点。
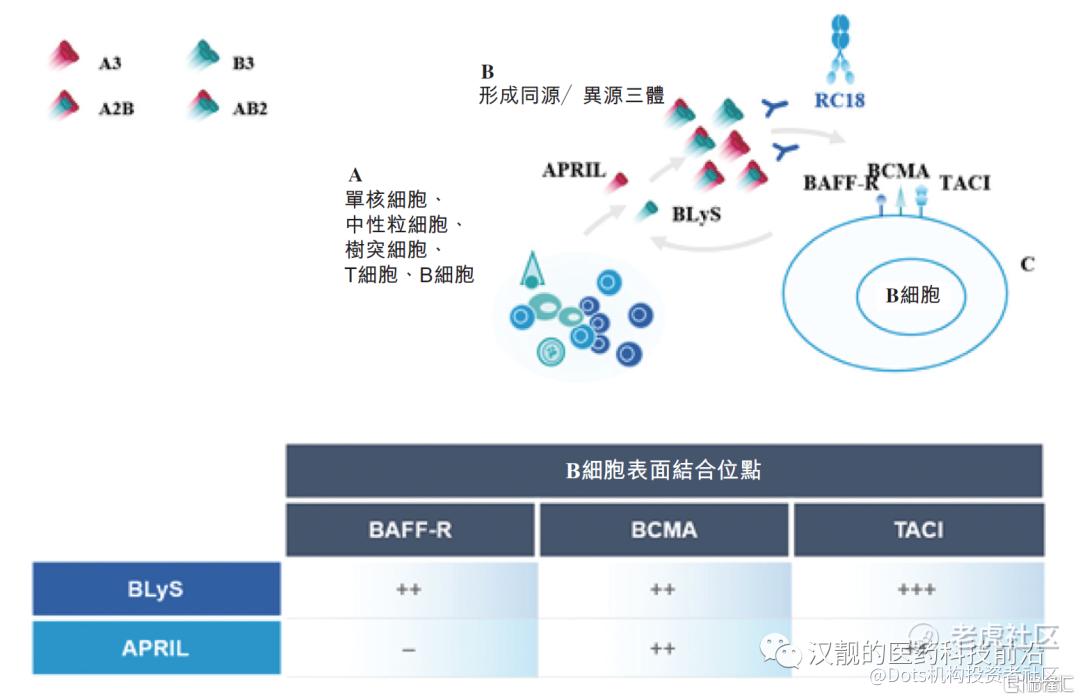
细胞因子BLyS和B细胞表面的BAFF-R、BCMA以及TACI相结合,而细胞因子APRIL和B细胞表面的BCMA及TACI结合。从图2可知,泰它西普通过阻断BLyS和APRIL和B细胞表面的配体结合,从而抑制BLyS和ARIL信号通路传导。
图2:泰它西普的作用机理
资料来源:泰它西普招股书;注:A3=APRIL同源三聚体;B3=BLyS同源三聚体;A2B=两种APRIL以及一种BLyS分子中的异源三聚体;AB2=一种APRIL以及两种BLyS分子的异源三聚体。
目前,泰它西普进展最快的适应症:SLE在中国已递交上市申请(被纳入优先审批),同时美国FDA也同意泰它西普在美国进行针对SLE的注册性临床。此外,泰它西普在类风湿性关节炎(RA)和视神经脊髓炎频谱系(NMOSD)在国内也进入了关键性临床,同时也在积极的拓展其他领域的适应症,比如lgA,干燥综合征,多发性硬化症以及重症肌无力等。
1.2 泰它西普的临床研究数据
泰它西普递交NDA,是基于一项在中国进行的治疗SLE的临床IIb期注册性研究:多中心、随机、双盲及安慰剂对照,共入组249名中度至重度的SLE患者,主要临床终点是48周SLE应答者指数4(简称:SRI-4)响应的患者比例。
这里解释一下SRI-4:是SLE临床试验中用于评价疾病活动性及对治疗出现反应的联合终点,包含三个国际认可指数的标准,分别是SELENA-SLE疾病活动性指数(SELENA-SLEDAI),不列颠群岛狼疮评估小组(BILAG)以及医师全球评估(PGA)。
1) 安全性数据
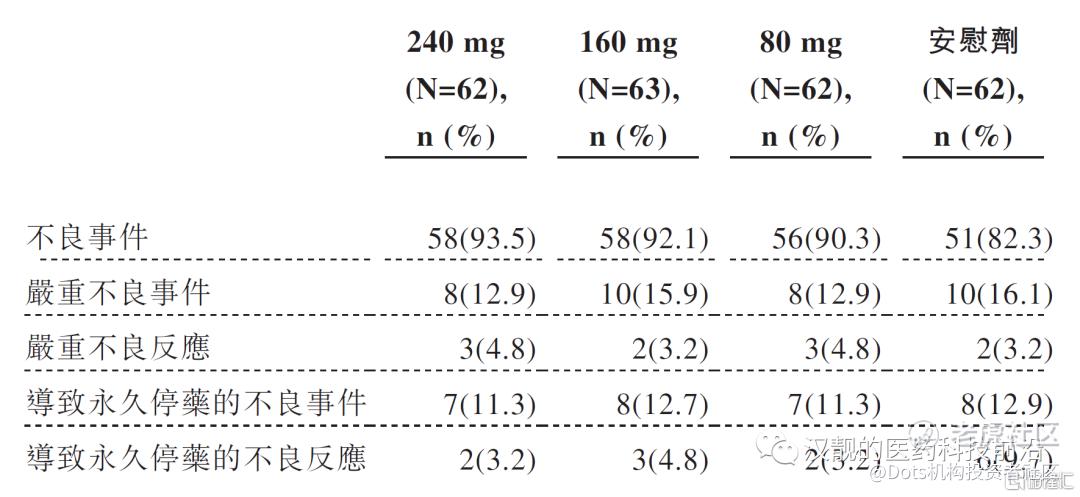
图3:泰它西普临床IIb的安全性数据
资料来源:荣昌招股书
对249名患者进行的临床IIb研究的安全性结果如图3所示,可以总结出,三个剂量组的泰它西普的严重不良事件和反应的比例都和安慰剂差不多,展示了泰它西普良好的安全性和耐受性。
2) 有效性结果
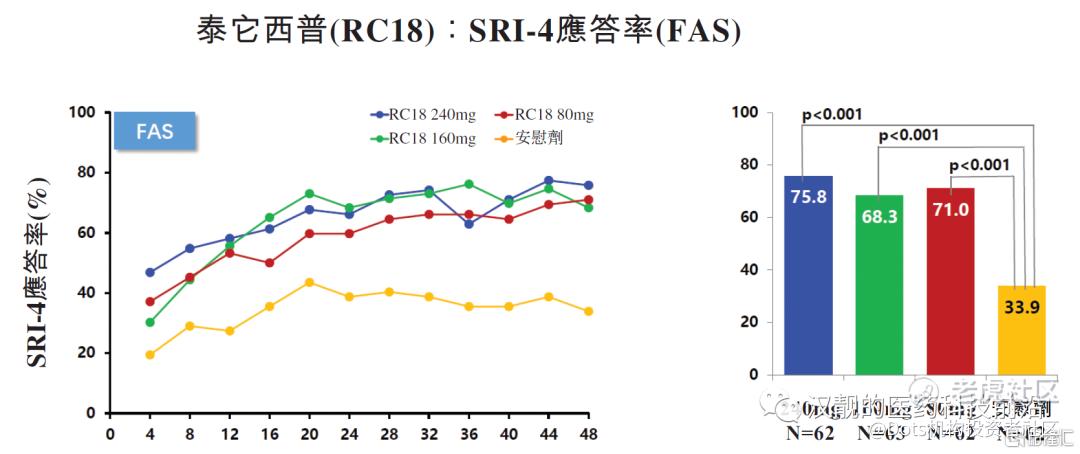
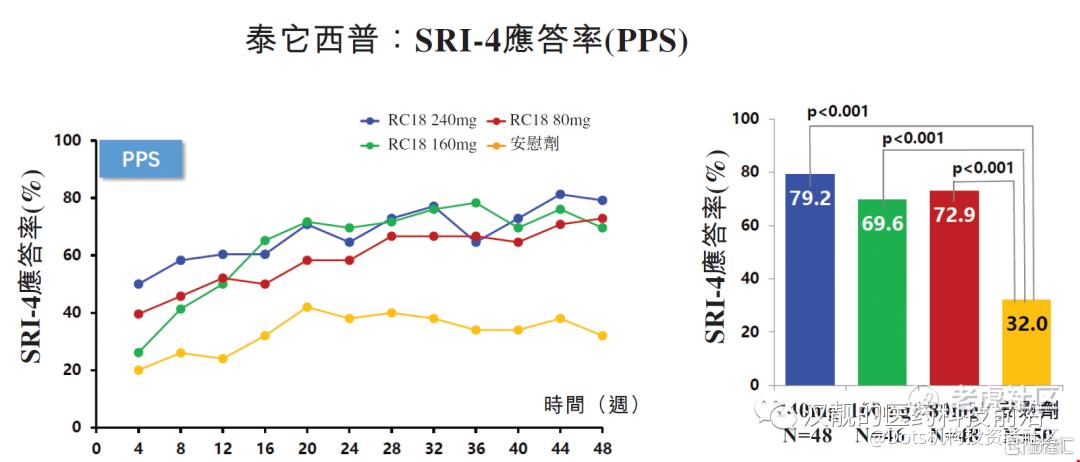
有效性结果表明(如图4):在FAS(全分析集:包括全部249名患者)和PPS(符合方案集:包括192名随机患者,患者已接受至少12剂泰它西普并完成SRI-4评估)分析中,接受泰它西普治疗的所有三个剂量组的患者,48周的SRI-4应答率都显著高于安慰组。其中,在FAS分析中,泰它西普240mg、160mg、80mg和安慰机组的48周SRI-4的响应率分别是75.8%、68.3%、71.0%和33.9%。
由于临床IIb达到了主要临床终点,荣昌已经基于该研究申请有条件批准泰它西普用于治疗SLE,并被授予优先审批资格,同时荣昌正在进行一项验证性III期,评估泰塔西普和标准疗法联用治疗SLE。
图4:泰它西普在SLE临床IIb期的有效性结果(FAS分析和PPS分析)
资料来源:荣昌招股书
第二部分:FDA近60年唯一获批的SLE新药:贝利尤单抗的原理和临床数据
2.1 贝利尤单抗介绍
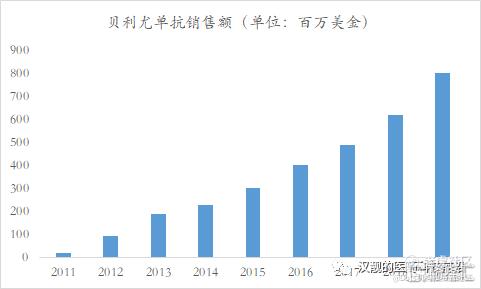
作为唯一一款FDA批准、治疗SLE的生物制剂Benlysta(倍力腾;通用名:Belimumab),和我们上面提到的泰它西普靶向两个细胞因子不同,Benlysta仅靶向B淋巴细胞刺激因子BLyS,且是一款全人源单抗药物,用于治疗自身抗原呈阳性,且正在接受标准治疗方法五岁及以上的活性SLE患者,2011年贝利尤单抗的静脉剂在美国上市,2017年皮下注射剂获批。Benlysta销量如图5所示,2019年收入约为8亿美金,其中美国市场占比87%。
图5:贝利尤单抗的销售额
资料来源:GSK
2.2 贝利尤单抗的安全性数据
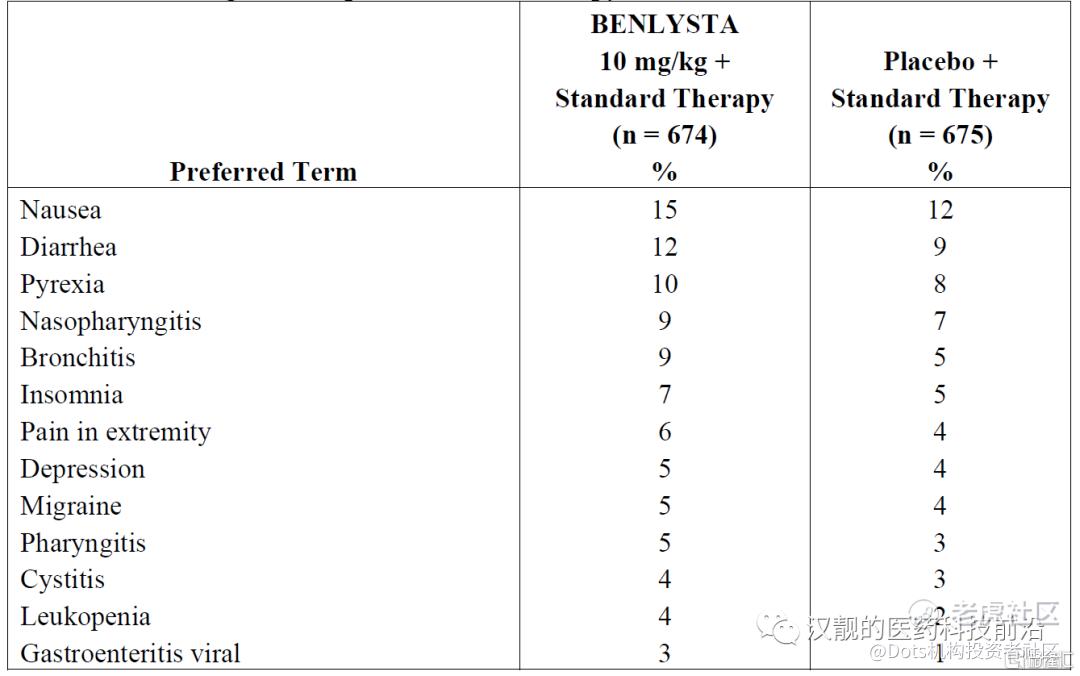
图6展示了贝利尤单抗的安全性数据(来自三个不同的有对照组的研究),整体来说,贝利尤单抗耐受性良好,没有明显的毒性,常见的副作用包括恶心、腹泻和发热。
图6:贝利尤单抗的安全性数据
资料来源:FDA
2.3 贝利尤单抗的有效性数据
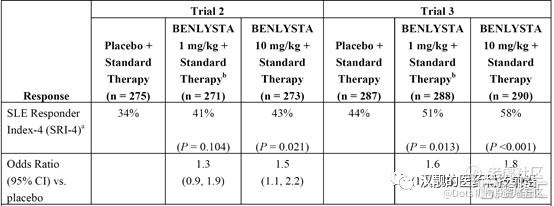
贝利尤(静脉注射剂型)的安全性和有效性是在三个大型的随机、双盲、安慰剂为对照的研究中进行评价的,共入组2,133名患者,分别是Trials 1、2和3。其中Trial 2和Trial 3的主要临床终点,和我们前面介绍泰它西普临床IIb期的研究一样,都是采用SRI-4综合指标,不过治疗的时间略有不同,是第52周进行评价,其有效性结果如图7所示。
图7:贝利尤两项临床III期的有效性结果
资料来源:FDA
从图7可以总结出,在Trial 2和Trial 3中,Benlysta(10mg/kg)和标准疗法的联用相比于安慰剂+标准疗法联用,第52周的SRI-4响应率都有了显著提高。
2.4 贝利尤单抗超过十年的跟踪研究结果
Arthritis & Rheumatology在2019年刊登了一项对于接受贝利尤治疗SLE长达13年的跟踪研究(Daniel Wallace et., Safety and Efficacy of Belimumab Plus Standard Therapy for Up to Thirteen Years in Patients With Systemic Lupus Erythematosus, 2019)。
结果表明:对于298名进入到“贝利尤持续研究”的患者中,截止至研究结束,96名患者(32.3%)依然留在研究中,其中5年、7年和10年留在研究中接受治疗的患者比例分别是70.1%,60.1%和44.3%。
有效性结果显示:达到SRI响应患者的比例从第一年16周的32.8%(88/268),上升至第12年32周的75.6%(68/90),展示了贝利尤持续的有效性。此外,长期跟踪研究表明贝利木单抗耐受性良好,没有新的安全问题。该研究是目前为止,评价贝利尤单抗治疗SLE最长时间的跟踪研究。
关于Benlysta的适应症拓展(资料来源:GSK官网),包括单药在Lupus Nephritis(狼疮性肾炎)已完成注册临床并达到主要临床终点,另外,和CD20单抗利妥昔联用治疗SLE和SS(干燥综合征),分别进入临床III期和临床II期。
第三部分:SLE领域具有代表性的在研或停止研发的生物药
长久以来,SLE作为一种自体免疫疾病,由于疾病本身的异质性、发病机制不明等原因,开发 SLE的新药一直充满挑战,面对着全球500万的SLE人群,传统的治疗方式包括糖皮质激素、抗疟疾药、免疫抑制剂等等,存在着巨大的未满足的临床需求。那么除了已经获批上市Benlysta,以及本文第一部分介绍的已经递交上市申请的荣昌的泰它西普,还有哪些具有代表性的在研或者是停止研发的SLE生物制剂呢?
3.1 AZ的MEDI-546(Anifrolumab):历经波折,即将NDA
Anifrolumab是阿斯利康在研的一款靶向I型干扰素受体的全人单抗,该靶点的选择基于超过50%的成人SLE患者拥有增高的干扰素水平。Anifrolumab已完成两项注册临床III期,AZ计划今年下半年递交上市申请,而这款药物的研发也可以说是一波三折。
2018年,AZ宣布Aniforlumab在注册临床III期的TULIP 1中,未达到主要临床终点(12个月后的SRI-4响应率),紧接着,公司更改了另外一个临床III期TULIP 2的设计方案,把主要临床终点修改为52周的BICLA指标,并在2019年底宣布达到了主要临床终点,即BICLA的响应率:治疗组vs 安慰剂=47.8% vs 31.5%。
不过最终Aniforlumab能够成功获批,还具有一定的不确定性。
3.2 UCB和Biogen的Dapirolizumab pegol(简称DZP):已启动临床III期
UCB和Biogen的DZP是一款靶向CD-40配体的Fab类抗体药物。尽管在2018年,两家公司宣布DZP在一项针对SLE的临床IIb研究中,未达到主要临床终点(24周的BICLA指标),但因为在研究中,DZP展示了一定的有效性,在今年3月,两家公司决定启动DZP在SLE领域的临床III期。该临床III期(NCT04294667)计划入组450名中度到重度的SLE患者,主要临床终点是48周的BICLA响应率。
3.3 德国默克的阿塞西普(Atacicept):IIb未达临床终点
德国默克的阿塞西普(Atacicept),和我们本期节目的主角泰它西普一样,也是一款TACI-Fc融合蛋白,且同样靶向BLyS和APRIL。Atacicept最初由Biotech公司ZymoGenetics研发,后转让给德国默克。
2016年11月,德国默克宣布在一项评价Atacicept治疗SLE的临床IIb期研究中,主要临床终点(24周的SRI-4响应率)没有达到。不过德国默克指出,在对主要终点进行敏感性分析表明,当采用治疗第一天作为基线(而不是患者筛选访视作为基线),Atacicpt相比于安慰剂,SRI-4响应率的提高有显著差异。此外,对于病情高度活跃患者的亚组分析,也展示了Atacicept的有效性。不过尽管如此,如果我们现在翻看德国默克的最新pipeline,Atacicept在SLE领域的进展依然停留在临床II期。
3.4 强生的乌司奴单抗:今年6月宣布折戟针对SLE的临床III期
今年6月份,强生宣布暂停乌司奴单抗(商品名:喜达诺,Stelara;靶向IL-12和IL-23)在SLE领域的临床III期研究LOTUS,主要因为中期有效性分析显示乌司奴单抗治疗SLE缺乏有效性。LOTUS是一个全球,随机,双盲,安慰剂控制的临床III期研究,入组了516名活性SLE患者,主要临床终点是52周的SRI-4响应率。
虽然乌司奴已成为强生旗下的重磅药物,2019年销量超过40亿美金,且获批多个自体免疫领域的适应症,但此次却止步于SLE领域的临床III期。
除此之外,其他针对SLE的在研生物药还包括安进的AMG-570(靶向BLyS和ICOSL)、诺华的 VAY736(靶向BAFF-R)等等,这里就不展开讨论的。
最后总结一下本期的内容:本期从荣昌生物的核心产品泰它西普谈起,向大家介绍了贝利尤单抗及其他一些具有代表性的针对SLE的生物制剂,一方面看到贝利尤长达13年的跟踪研究展示的持续有效性,另一方面,也看到了开发SLE新药的挑战,即使是已经递交NDA的来自阿斯利康的Anifrolumab在两个临床III期也是一个失败一个成功,另外,UCB和Biogen的DZP更是在临床IIb不利的情况下启动三期。
此外,除了BlyS和APRIL属于SLE新药的热门靶点,该领域的热门靶点还包括I型干扰素受体、CD-40配体等,而由于SLE疾病的异质性,临床终点的选择也至关重要,甚至决定临床试验的成功或失败。
以上就是本期节目的全部内容,感谢大家的收听/收看!
本文转自微信公众号“汉靓的医药科技前沿”,原文地址为https://mp.weixin.qq.com/s/af5b_6hjlTwDlylM84tX-A
-END-
Dots社区现已入驻:
今日头条/扑克财经/见闻见识/**/36氪/富途牛牛/老虎社区/大风号/新浪微博/腾讯自选股/财富号/百家号……

精彩评论