“华兴资本医疗与生命科技行业周报”定期发布,专注从资本角度解读一周数据,并提供最新行业观察。
医疗与生命科技是华兴资本多年来关注并深耕的领域,目前已为近200个融资及并购项目担任财务顾问。
医疗与生命科技行业创新不断涌现,已经发展成为最活跃的行业之一;华兴资本始终支持、陪伴这一领域创业企业成长,致力为行业带来理性专业的声音。
作 者 | 华兴资本医疗与生命科技团队
关注华兴资本微信公众号(ID:iChinaRenaissance),后台点击“兴观点”-“行业观察”-“生命科技”,获取更多医疗与生命科技行业相关信息。
百明信康完成超3亿元D+轮融资,持续深耕过敏免疫疗法及自免领域并加速国际化布局
国内领先的过敏免疫疗法创新企业百明信康近日宣布完成超3亿元人民币D+轮融资。本轮融资由人保资本、LongRiver江远投资联合领投,深投控资本、千帆企航基金、合肥高投等多家知名投资机构及基金跟投,原有股东清松资本,明沣资本等亦持续加持。
行业视角:
本次融资获得多家知名资本的强力背书,充分体现了资本市场对百明信康技术平台、产品管线与全球商业化前景的高度认可。募集资金将主要用于核心产品的全球临床试验推进,并加速已商业化产品及在研管线的国际化布局。
信息来源:动脉网
碧利医疗完成数千万元新一轮融资,打造国内领先的显微手术器械解决方案
近日,国内眼科显微手术器械领域领导品牌—苏州碧利医疗科技有限公司(以下简称“碧利医疗”)正式宣布完成新一轮数千万元的融资。本轮融资由普华资本领投,深岩创投跟投。本次所融资金将用于显微手术器械智能制造中心的建设,眼科智能设备和耗材项目落地及海外市场销售拓展。
行业视角:
碧利医疗成立于2017年,专注于二、三类眼科、耳鼻喉科等全系列显微手术器械套包研发生产与销售。创始团队曾是全球眼科显微手术器械领导品牌在国内首选的OEM合作伙伴。进入自主品牌发展阶段后,碧利医疗逐步组建起国际化的研发团队,其中包括来自瑞士的眼科手术耗材专家和德国的光学设备专家,积累了跨领域多维度的产品设计与开发能力,实现了向自主知识产权设计的转型。
信息来源:动脉网
佩德生物完成数千万元A轮融资
2025年12月19日,专注于多肽药物研发的成都佩德生物医药有限公司宣布完成数千万元A轮融资。本轮融资由深圳前海上善金石私募股权投资基金管理有限公司旗下善诺基金独家投资。
行业视角:
公司本轮所募集资金将用于推进疼痛类、心脑血管类和呼吸系统疾病的核心管线研发,同时部署大规模人工智能(AI)辅助多肽药物开发技术。
信息来源:新浪网
微何生物完成首轮融资,聚焦合成生物制造赛道
北京微何生物科技有限公司(以下简称“微何生物”)宣布完成种子轮融资。本轮融资由专注于生命科技领域投资的泉华Life领投。所筹资金将主要用于研发平台搭建,科研团队建设,核心产品中试量产,加速高附加值食品新原料的生物制造,为大健康产业提供更加可持续的解决方案。
行业视角:
微何团队拥有丰富的底盘细胞诱变筛选、定向进化经验,以及优秀的转化落地执行力;尤其在功能性蛋白、糖苷类与天然多酚类等产品管线已处于从实验室到产业化开发的关键时期。此次所筹资金将主要用于底盘细胞开发、工艺优化以及渠道布局等方面,助力企业合成生物技术快速发展。
信息来源:动脉网
领泰生物完成超2亿元B轮融资,加速产品临床研究
2025年12月18日,领泰生物医药有限公司宣布成功完成超2亿元B轮融资。本轮融资由汉康资本领投,鼎晖VGC、时真资本、康橙投资等投资机构共同参与,老股东龙磐投资持续追加投资。
行业视角:
本轮所融资金将主要用于加速公司核心管线的临床开发与研发平台升级,具体包括:推动首个核心产品——IRAK4降解剂LT-002,加快Ic期适应症探索及II期临床研究;启动第二个核心产品--KRAS G12D降解剂的I期临床试验;加速其他自免管线和肿瘤管线的临床前开发;支持研发中心的全面运营,并进一步扩充研发团队。
信息来源:新浪网
荷声科技完成Pre-A轮融资,专注于微型片上超声模组与系统
2025年12月18日消息,荷声科技完成Pre-A轮融资,由阿斯利康中金医疗产业基金领投,中芯聚源、杭州高新金投、上海拙朴等机构共同参与。
行业视角:
荷声科技专注于微型片上超声模组与系统,荷声科技(Sonosilicon)依托面阵ASIC、硅基超声换能器与基于边缘计算的超声AI,构建从芯片、模组到智能系统的自主技术链。
信息来源:投资界
只等特朗普签字,美国《生物安全法案》即将生效!
继上周在众议院获得投票通过后,搭载修订版《生物安全法案》的美国2026财年《国防授权法案(2026NDAA)》,于北京时间12月18日凌晨,以77票赞成、20票反对的结果,在参议院获得通过。至此,2026NDAA现已完成国会两院的主要立法程序即将送往白宫,由美国总统签署后立即生效。
• 罗氏Gazyvaro获欧盟批准用于治疗狼疮性肾炎
• FDA授予BMS单抗联合疗法优先审评审批资格
• 恒瑞医药多款新药获批临床 覆盖肥胖、肿瘤、前列腺癌等多个治疗领域
• GSK重度哮喘新药获FDA批准上市
• 国产流感新药赛道再添新玩家 健康元玛帕西沙韦胶囊获批上市
• 多款医疗器械产品获批上市
罗氏Gazyvaro获欧盟批准用于治疗狼疮性肾炎
12月9日,罗氏官网宣布欧盟委员会批准其Gazyvaro(奥妥珠单抗)联合标准治疗用于治疗成人狼疮性肾炎(LN),这是Gazyvaro在欧盟的首个新适应症。此前,该药已在美国获得类似批准,由罗氏与Biogen合作并以Gazyva为商品名销售。
信息来源:动脉网
FDA授予BMS单抗联合疗法优先审评审批资格
12月11日,BMS官网宣布美国食品药品监督管理局(FDA)已受理并授予Opdivo®补充生物制品许可申请(sBLA)优先审评资格,Opdivo单抗联合多柔比星、长春碱和达卡巴嗪(AVD方案)用于治疗既往未接受治疗的成人和儿童(12岁及以上)III期或IV期经典型霍奇金淋巴瘤(cHL)患者。
信息来源:动脉网
恒瑞医药多款新药获批临床 覆盖肥胖、肿瘤、前列腺癌等多个治疗领域
恒瑞医药(600276/01276)发布公告,公司及旗下子公司近期收到国家药品监督管理局核准签发的多款药物《药物临床试验批准通知书》,获批药物涵盖治疗用生物制品、化药新药及仿制药,适应症覆盖超重肥胖、多发性骨髓瘤、前列腺癌等多个治疗领域。
信息来源:财中社
GSK重度哮喘新药获FDA批准上市
GSK宣布,美国FDA批准Exdensur(depemokimab)作为附加维持治疗药物,用于治疗以嗜酸性粒细胞表型为特征的重度哮喘,适用于12岁及以上的成人和青少年患者。根据新闻稿,Exdensur是首个获批用于嗜酸性粒细胞表型重度哮喘患者、且每年仅需给药两次的超长效生物制品。
信息来源:搜狐
国产流感新药赛道再添新玩家 健康元玛帕西沙韦胶囊获批上市
近日,健康元公告称,公司旗下1类创新药玛帕西沙韦胶囊(壹立康)正式获批上市。该药物为抗流感1类新药,适用于既往健康的12岁及以上青少年和成人单纯性甲型和乙型流感患者的治疗,不包括存在流感相关并发症高风险的患者。据悉,玛帕西沙韦胶囊为“一次口服完成全疗程”的新型帽依赖性核酸内切酶抑制剂,全病程仅需服用一次,临床依从性有所提升。
信息来源:财联社
多款医疗器械产品获批上市
雅培双重获批,结构性心脏病封堵器集采落地
雅培宣布其Amplatzer Piccolo™ Delivery System同时获FDA批准与CE认证,用于优化早产儿动脉导管未闭(PDA)的经导管治疗流程。为结构性心脏病微创介入在极低体重人群应用提供新工具。PDA是常见先天性心脏病,胎儿期动脉导管出生后未闭合会形成持续左向右分流,加重呼吸负担,引发呼吸困难等问题,其症状与导管大小等因素相关,严重者诊断处理失当危及生存。PDA治疗从外科结扎发展到经导管封堵技术,但早产儿尤其是极低体重者治疗长期面临挑战,约20%早产儿PDA需干预治疗,专用解决方案有明确临床需求。Amplatzer Piccolo™ Delivery System专为早产儿设计,配合Amplatzer Piccolo™ Occluder使用。
信息来源:心未来
水木青创助力华融科创合利多卡因注射用交联透明质酸钠凝胶取证
12月10日,水木青创助力Adoderm GmbH研发、华融科创代理的“合利多卡因注射用交联透明质酸钠凝胶Hyabell Ultra”获NMPAⅢ类进口医疗器械批准,该产品用于面部真皮中层注射以纠正中重度皱纹。合作中,水木青创提供临床试验全流程服务。Adoderm GmbH是德国专业生产医疗器械的高科技企业,主营整形外科和皮肤科领域产品。华融科创是科创医疗集团研发生产总部基地,以解决临床痛点为导向,提供创新解决方案。北京水木青创医药科技有限公司是专注为医疗器械企业提供专业临床研究技术服务的CRO,总部位于北京,在多地设立分公司并派出人员,团队经验丰富,优势领域广泛,与全国200多家优秀临床研究中心合作,服务客户超200家。
信息来源:中关村水木医疗
TroClose 2.0:带缝合功能的腹腔镜穿刺器获FDA批准上市零切口疝发生率
Gordian Surgical宣布其带缝合功能的腹腔镜穿刺器TroClose 2.0获FDA批准上市。腹腔镜手术切口疝发生率高达7%,传统闭合方法成本高且耗时,TroClose 2.0能将切口疝发生率降至0%,杜绝患者切口疝发生。其他临床研究显示,该产品不仅减轻术后患者疼痛,术后12个月穿刺孔处切口疝发生率为0%。TroClose 2.0包括套管和穿刺针,内置缝线和可吸收锚定,采用独特的180度缝线布放系统,组织张力显著降低75%,可降低患者术后一周疼痛感。此外,它还能实现自动化预设闭合,消除震动运动难题,确保闭合更顺畅精准,且是市场上唯一无需维持气腹或可视化就能安全高效闭合穿刺孔的产品。
信息来源:MedTF
TRUFILL n-BCA:继美敦力之后,强生液态栓塞剂新适应症获FDA批准上市
强生宣布其液体栓塞剂TRUFILL n-BCA新适应症获FDA批准,用于脑膜中动脉栓塞术治疗症状性亚急性与慢性硬膜下血肿(cSDH),此前美敦力的Onyx LES也获批准同适应症。TRUFILL n-BCA新适应症获批基于MEMBRANE随机对照试验,研究显示其治疗有效性优于标准方案且安全性得到证实。专家评价其满足了慢性硬膜下血肿的治疗方案的需求,高管称此次获批见证产品价值,体现了公司承诺。慢性硬膜下血肿在老年及抗凝治疗患者中常见,传统手术复发率较高,脑膜中动脉栓塞术作为微创方法可治疗该疾病。TRUFILL n-BCA已有超25年历史,此次适应症扩大使其性能可应用于慢性硬膜下血肿治疗。
信息来源:MedTF
Hyperfine宣布Swoop系统在印度获得监管批准
Hyperfine, Inc.是一家以FDA认证的AI驱动便携式脑部MRI系统Swoop®闻名的健康技术公司,已获得印度中央药品标准控制组织(CDSCO)的监管批准。这一批准使得Swoop®系统能够在印度全国范围内商业化,满足了这一全球规模最大且增长最快的医疗市场对先进脑成像的重大未满足需求。Hyperfine将与领先医疗设备分销商Radiosurgery Global, Ltd.(RSG)合作分销该系统,RSG在先进医学影像领域拥有专业能力,并在印度医疗系统中具备强大的网络。RSG董事总经理Kapil Kalra强调,此次合作将把Hyperfine 创新的便携式脑部MRI技术转化为可扩展的解决方案,推动其在印度的广泛应用,从而提升全国神经影像服务的提供方式和覆盖范围。尽管印度相对于其超过14亿的人口MRI基础设施有限,但该国仍是改善神经影像获取途径的一个重要全球机遇。
信息来源:AIHIM
获批FDA,新一代腔镜手术机器人
2025年12月17日,CMR Surgical宣布其Versius Plus机器人辅助手术系统在美国FDA 510(k)批准,可用于胆囊切除等软组织微创手术,此批准建立在此前通过FDA De Novo审查基础上,标志着CMR在美国监管路径的关键进展。CMR Surgical成立于英国剑桥,产品策略区别于传统大型手术机器人,选择模块化、可扩展、贴近现有腹腔镜体系的技术路线,先在欧洲积累经验再推进美国市场。Versius Plus并非全新平台,是在原有架构上的系统级升级,重点在于“更好用、更好落地”。其延续模块化方案设计,机械臂灵活布置,降低医院改造成本;操作流程用开放式控制台,适应数字医院和多学科团队;成像与能量能力上,系统支持荧光成像。
信息来源:MedRobot
• 礼来创新药物匹妥布替尼在全球首个对比伊布替尼的头对头III期研究中成功达到主要终点
• 礼来创新药物匹妥布替尼显著延长初治CLL/SLL患者的无进展生存期
• 诺华公布一项BAFF-R单抗III期临床试验结果
• 再鼎医药双特异性抗体ZL-1503全球I/Ib期临床启动
• 信达生物匹康奇拜单抗一项新临床III期研究达成终点
• 康方生物PD-1/CTLA-4 双特异性抗体联合治疗胃癌国际Ⅲ期临床获FDA批准
礼来创新药物匹妥布替尼在全球首个对比伊布替尼的头对头III期研究中成功达到主要终点
礼来公司公布III期BRUIN CLL-314临床试验的最新结果。该研究旨在评估非共价(可逆)BTK抑制剂捷帕力®(匹妥布替尼)与共价BTK抑制剂亿珂®(伊布替尼)在初治或未经BTK抑制剂治疗的慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)患者中的疗效表现。结果显示,在意向治疗(ITT)人群中,匹妥布替尼在总体缓解率(ORR)方面达到非劣效性的主要终点,并在数值上优于伊布替尼。
信息来源:动脉网
礼来创新药物匹妥布替尼显著延长初治CLL/SLL患者的无进展生存期
礼来公司公布III期BRUIN CLL-313临床试验的最新结果。该研究旨在评估非共价BTK抑制剂捷帕力®(匹妥布替尼)与苯达莫司汀联合利妥昔单抗(BR)在不伴17p缺失的初治慢性淋巴细胞白血病或小淋巴细胞淋巴瘤(CLL/SLL)患者中的疗效与安全性。研究结果显示,匹妥布替尼将患者疾病进展或死亡风险降低80%(HR=0.20,[95% CI, 0.11-0.37];p<0.0001),达到主要终点。
信息来源:动脉网
诺华公布一项BAFF-R单抗III期临床试验结果
诺华公布了其BAFF-R单抗药物作为原发免疫性血小板减少症(ITP)二线治疗III期临床试VAYHIT2的详细数据。VAYHIT2是一项III期临床试验,旨在评估伊那鲁单抗联合艾曲波帕治疗既往接受过糖皮质激素治疗的原发性免疫性血小板减少症(ITP)患者的疗效。根据主要终点——治疗失败时间(TTF),伊那鲁单抗(9mg/kg)联合艾曲波帕治疗使ITP疾病控制时间延长了45%。诺华计划于2027年向卫生监管机构提交VAYHIT2二线ITP试验数据以及正在进行的一线ITP试验VAYHIT1的结果。
信息来源:动脉网
再鼎医药双特异性抗体ZL-1503全球I/Ib期临床启动
再鼎医药宣布,其自主研发的IL-13/IL-31R双特异性抗体ZL-1503,用于治疗特应性皮炎的全球I/Ib期临床研究已完成首例受试者给药。该研究旨在评估药物的安全性与有效性,其双重靶向策略有望为中重度患者提供更优的疗效。
信息来源:动脉网
信达生物匹康奇拜单抗一项新临床III期研究达成终点
近日,信达生物官网宣布,其自主研发的重组抗白介素23p19亚基(IL-23p19)抗体注射液匹康奇拜单抗(研发代号:IBI112)在中国中重度斑块状银屑病受试者中开展的随机撤药和再治疗III期临床研究(CLEAR-2)中达成主要终点和次要疗效终点。信美悦®作为首个中国原研的IL-23p19单抗,已于2025年11月获国家药品监督管理局(NMPA)批准用于适合系统性治疗的中重度斑块状银屑病成人患者。
信息来源:动脉网
康方生物PD-1/CTLA-4 双特异性抗体联合治疗胃癌国际Ⅲ期临床获FDA批准
12月12日,康方生物宣布公司全球首创的PD-1/CTLA-4 双特异性抗体卡度尼利单抗联合化疗,对比化疗联合或不联合纳武利尤单抗,用于HER2阴性、未经治疗的不可切除或转移性胃或胃食管结合部腺癌一线治疗的国际多中心Ⅲ期临床研究(COMPASSION-37/AK104-311),已获得美国食品药品监督管理局(FDA)批准开展。
信息来源:动脉网
• 48亿美元大收购,罕见病“军备竞赛”升级
• 国资重仓:国投控股生物制造细分龙头东圣生物
• 百万医疗险首次纳入专属康复责任,健嘉康复携手众安保险开启“保险+康复”新生态
• 5.01亿元!广药系收购+1
• 年产800万吨!全球首个玉米表达重组胶原蛋白平台,由美尚洁生物携手美国康奈尔海归博士后共同打造
48亿美元大收购,罕见病“军备竞赛”升级
12月19日路透社报道,BioMarin Pharmaceutical宣布以约48亿美元收购Amicus Therapeutics,收购价较Amicus前一日收盘价溢价33.1%。通过此次收购,BioMarin将获得Amicus旗下针对法布里病和庞贝病的治疗药物,丰富其罕见病治疗领域产品管线。资金方面,BioMarin计划用自有现金及37亿美元债务融资完成交易,并表示收购将立即带来收入增长,预计前12个月提升调整后利润,2027年起显著增厚收益。此次并购凸显了BioMarin深耕罕见代谢病领域的战略决心,有望强化其在全球罕见病治疗市场的竞争优势。此外,文章还提及三生国健核心技术人员离职、华人抗体协会专题报告及美国投行看好奥布替尼等消息。
信息来源:一度医药
国资重仓:国投控股生物制造细分龙头东圣生物
国家开发投资集团所属的国投生物制造创新研究院与泰兴市东圣生物科技有限公司签署股权转让协议,并启动新质蛋白产业化项目,最终国投生物制造创新研究院将控股东圣生物。据报道,国务院国资委2023年启动实施央企产业焕新行动和未来产业启航行动,聚焦生物制造、新材料等15个重点产业领域方向。
信息来源:动脉网
百万医疗险首次纳入专属康复责任,健嘉康复携手众安保险开启“保险+康复”新生态
健嘉康复与互联网保险龙头众安保险达成战略合作,宣布在众安保险尊享e生2026百万医疗保险产品中创新性纳入专属康复医疗责任。这是行业内首次将专业康复服务与百万医疗险深度融合,打破了传统商业保险医疗保障只保“治病”不管“康复”的痛点,为用户提供从临床治疗到术后康复的全周期医疗保障解决方案。
信息来源:动脉网
5.01亿元!广药系收购+1
广州白云山医药集团股份有限公司(A股:600332;H股:00874)发布公告,其控股子公司广州医药股份有限公司(新三板:874839)与浙江海正药业股份有限公司(股票代码:600267)正式签署股权交易协议,拟以5.005亿元受让海正药业所持浙江省医药工业有限公司100%股权。
信息来源:动脉网
年产800万吨!全球首个玉米表达重组胶原蛋白平台,由美尚洁生物携手美国康奈尔海归博士后共同打造
近日,江苏美尚洁生物科技有限公司与南京农业大学吴昊教授(曾任美国康奈尔大学植物学博士后)团队达成重磅研发合作。双方将共同推进“利用玉米籽粒生物反应器合成重组人源化胶原蛋白”的研发与产业化,旨在构建具有全球竞争力的生产平台,攻克重组人胶原蛋白高成本、难量产的行业痛点,以期全面替代动物源胶原蛋白,满足市场对高品质胶原蛋白的迫切需求。
信息来源:动脉网
重组蛋白龙头冲刺H股!
百普赛斯(股票代码:301080.SZ)发布公告,董事会已审议通过发行境外上市外资股(H股)并拟于香港联合交易所主板挂牌上市的相关议案。公告明确,此次资本动作核心目标是推进全球化战略布局、搭建国际化资本运作平台、提升综合竞争力。不过,具体发行规模、定价区间及发行时点仍在制定中,后续需提交股东大会审议,并获得相关政府及监管机构的批准与核准。
信息来源:动脉网
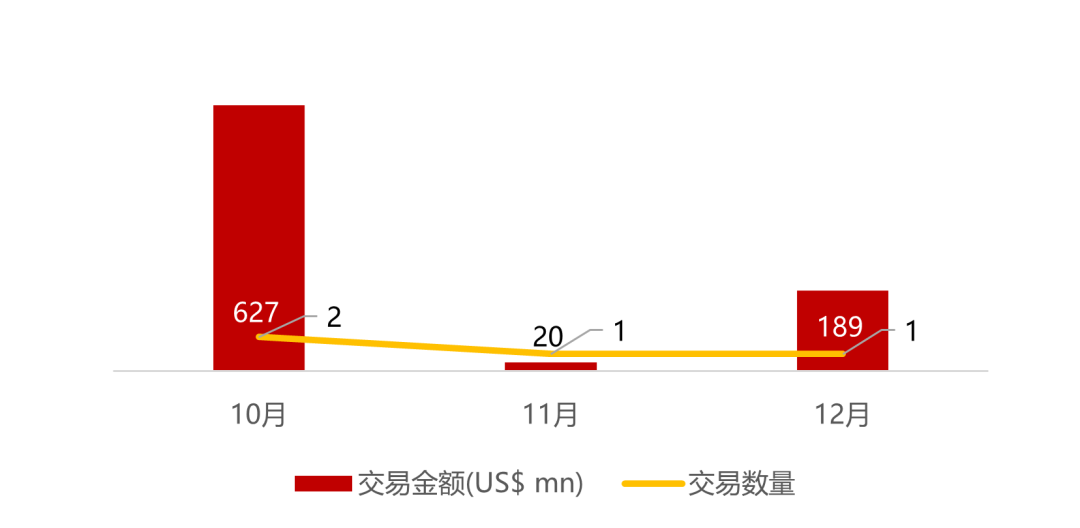
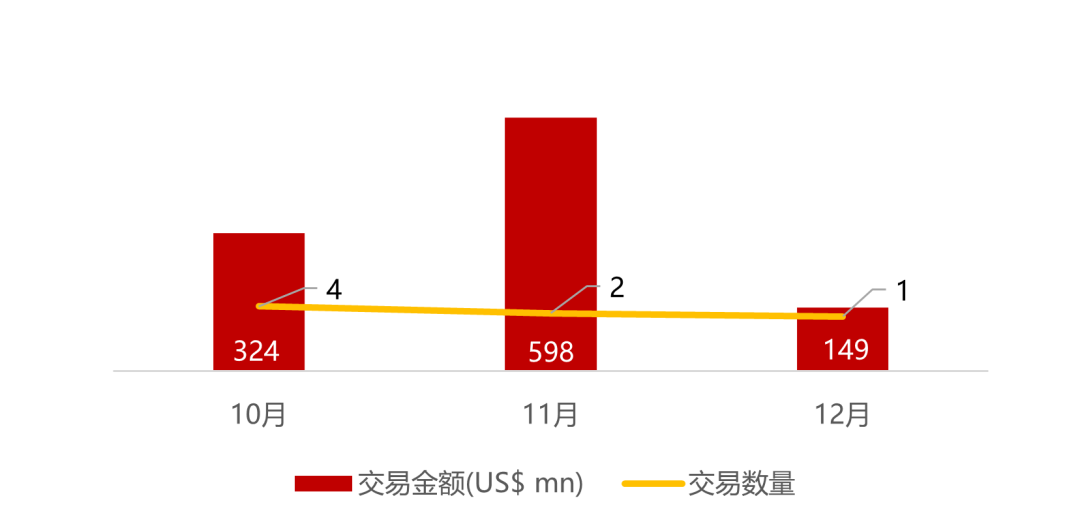
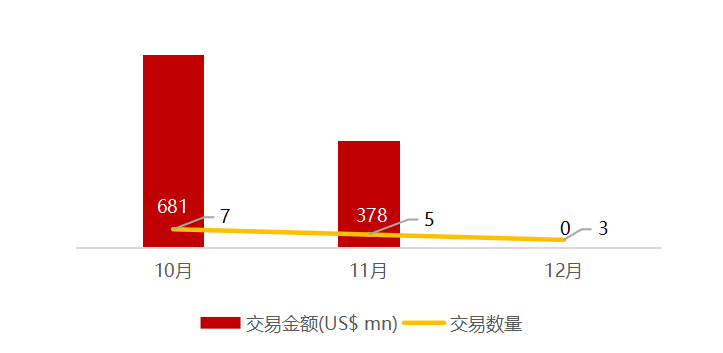
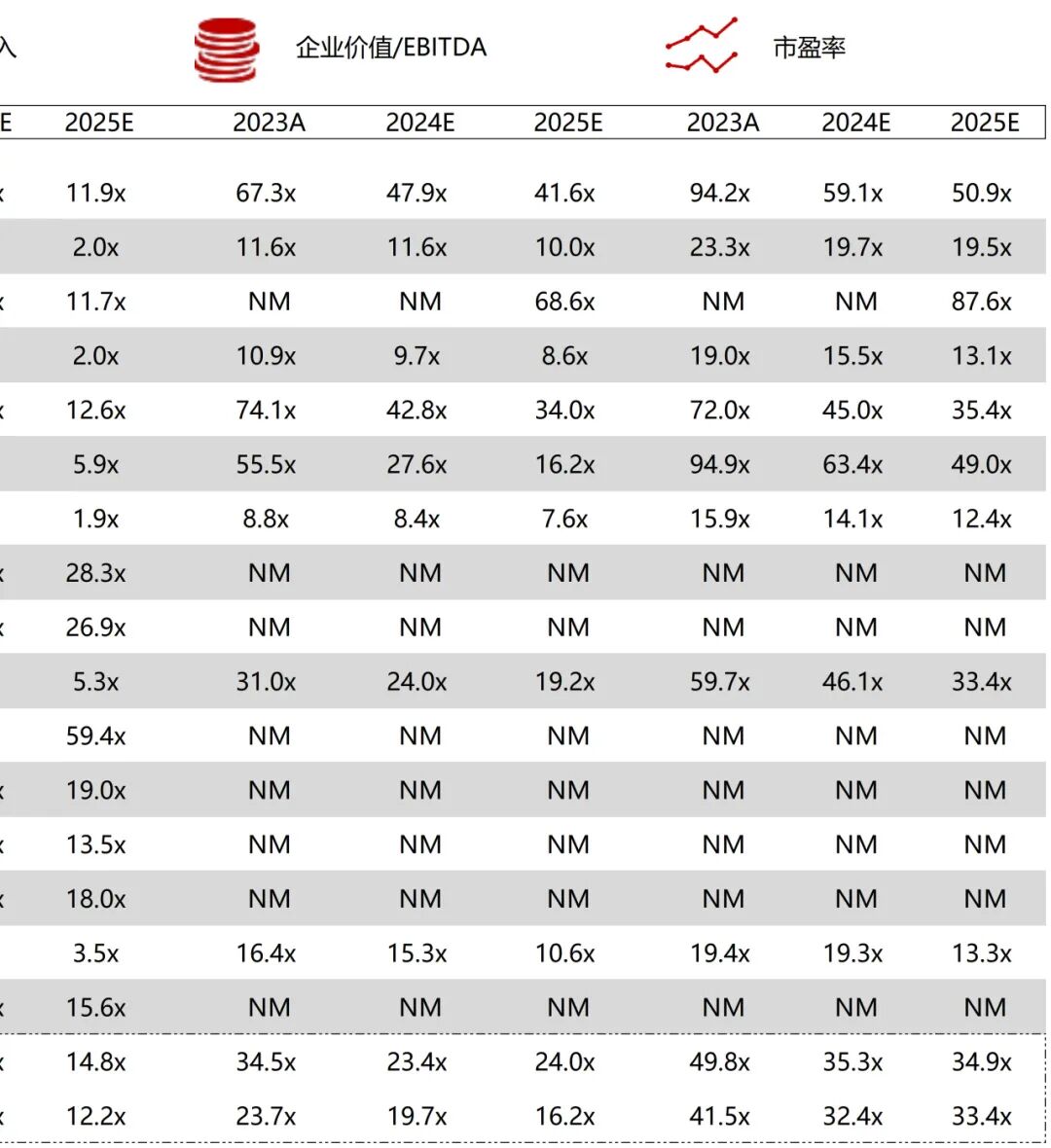
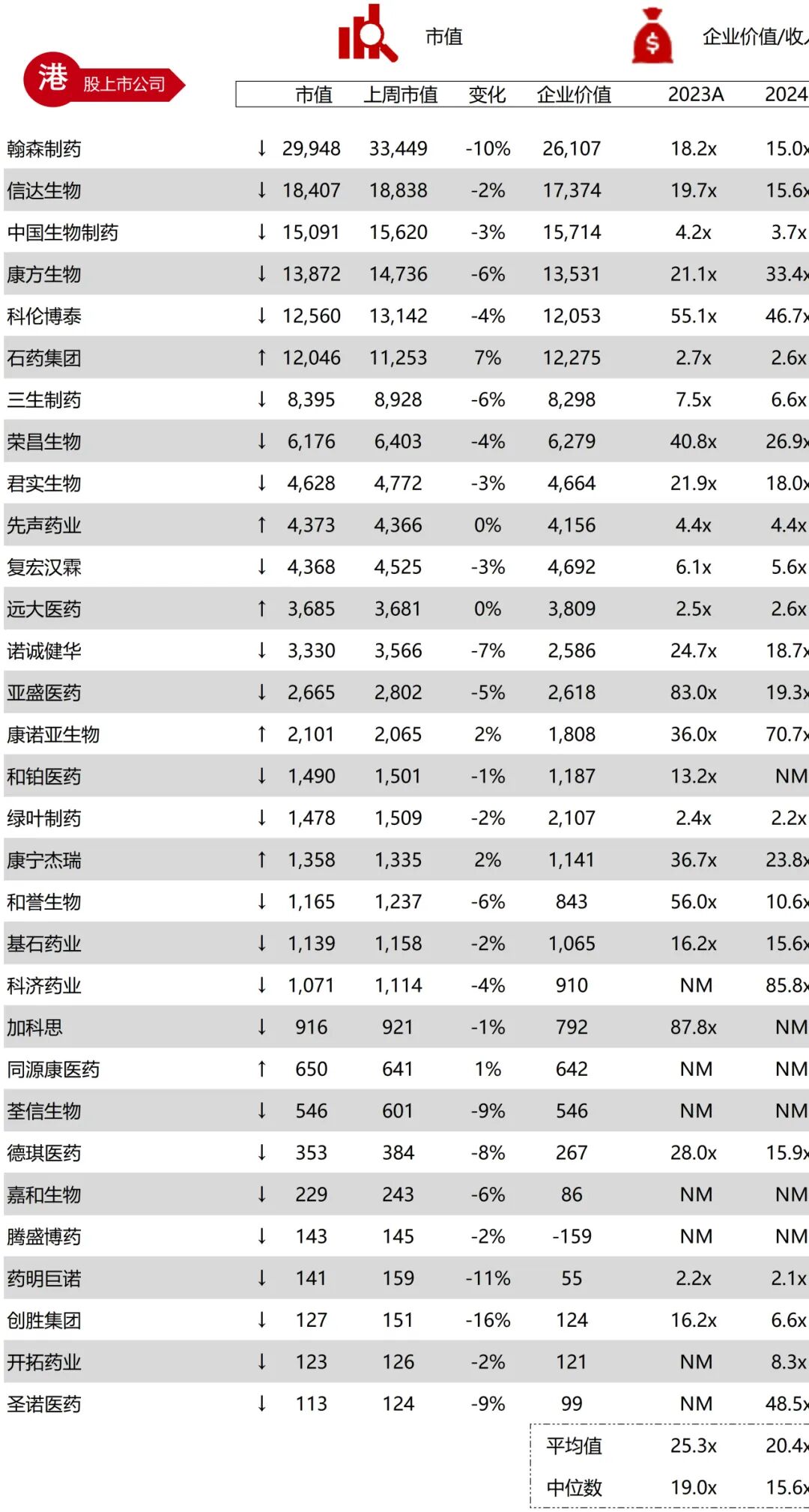
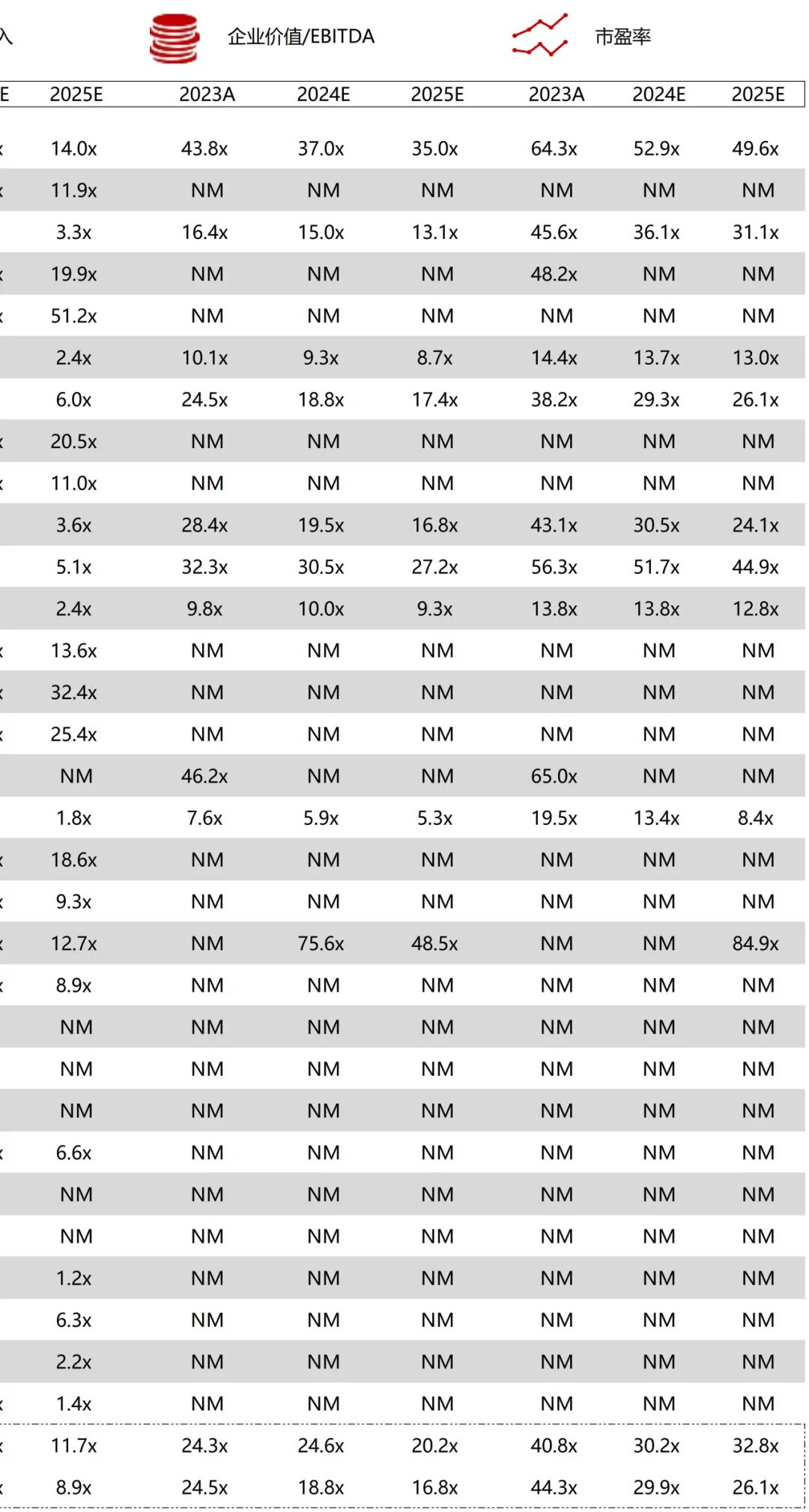
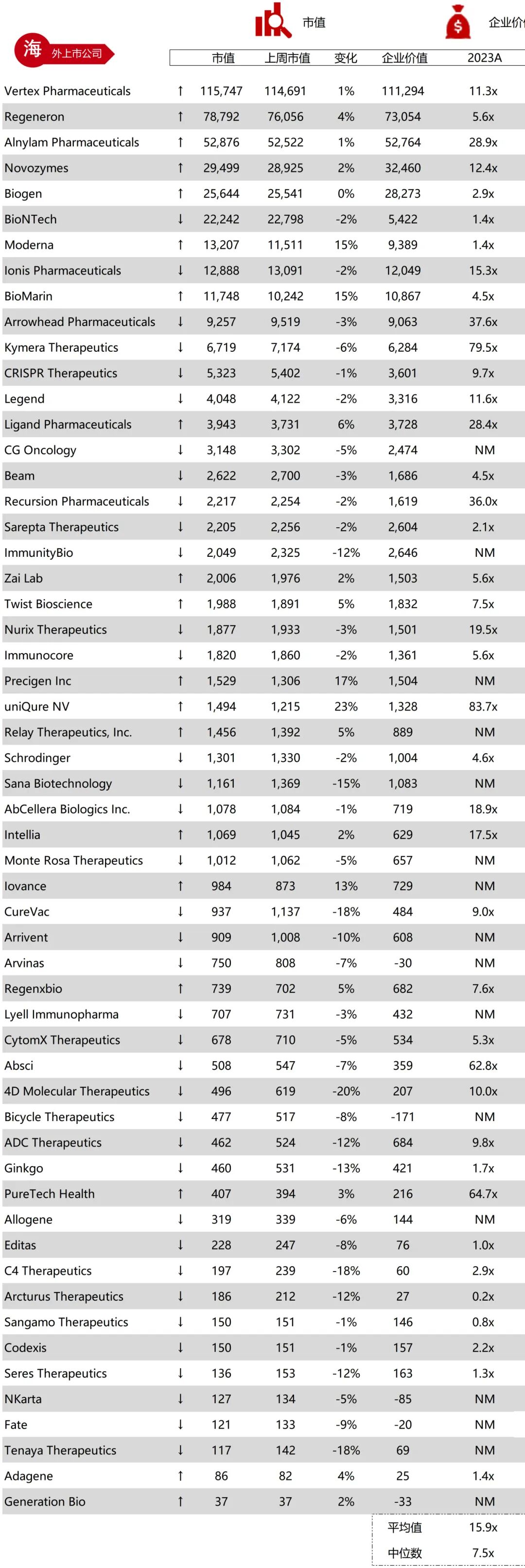
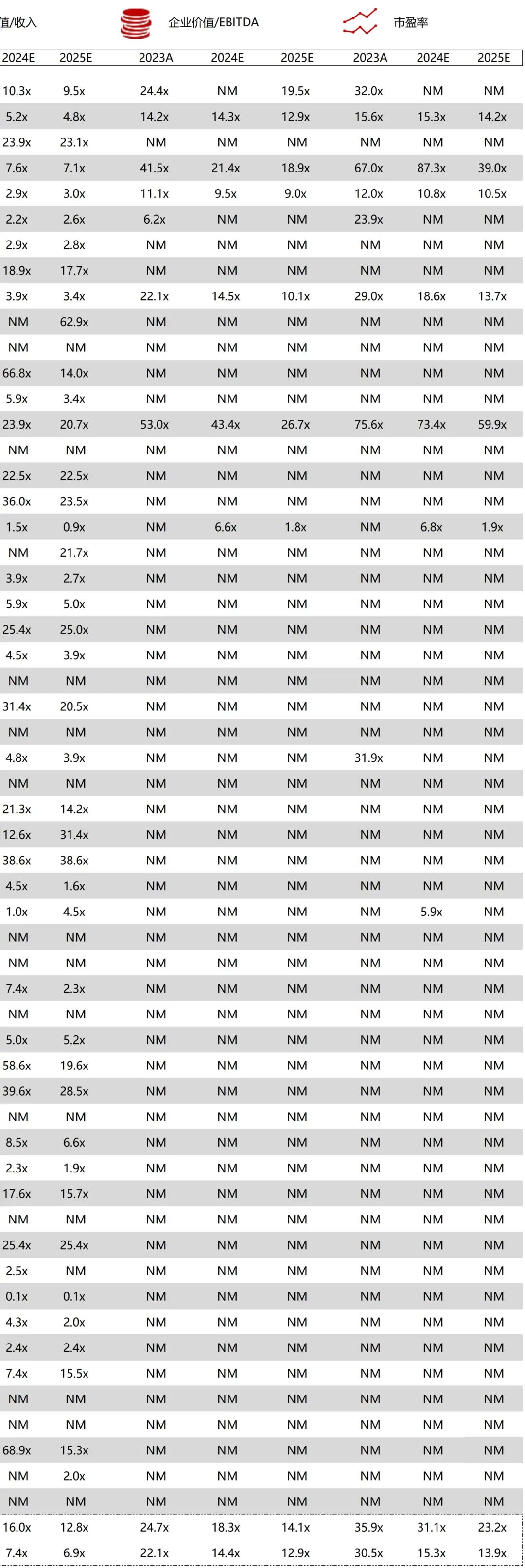
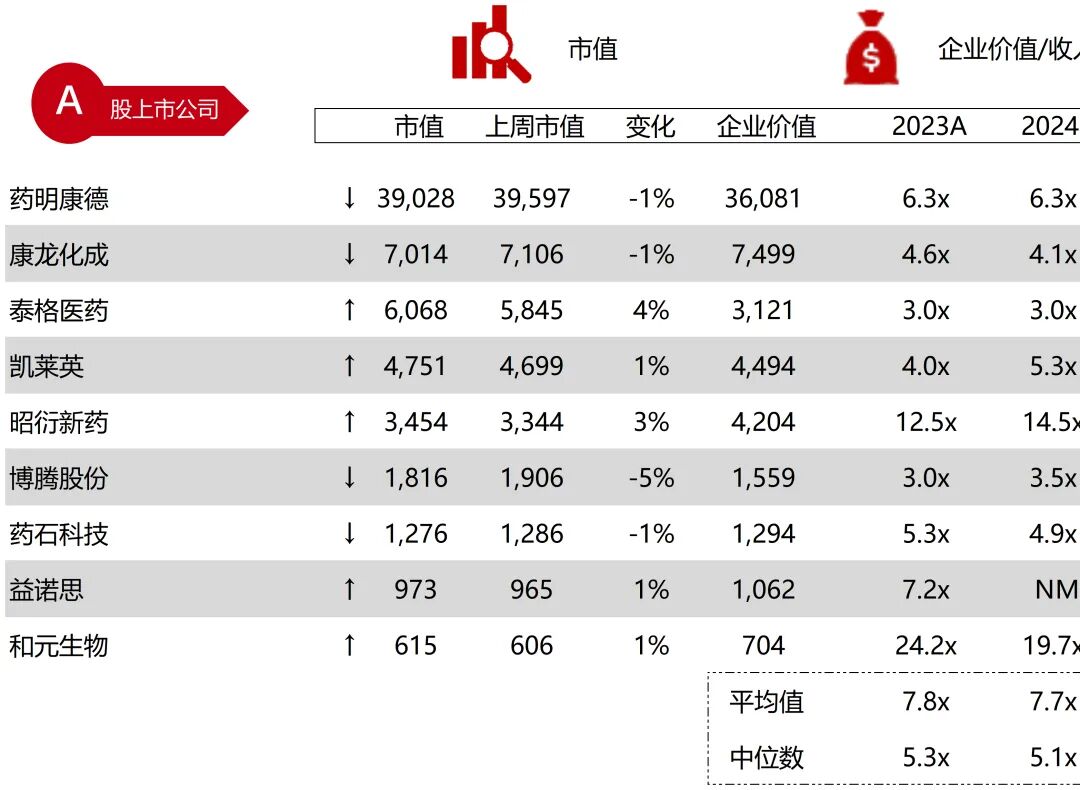
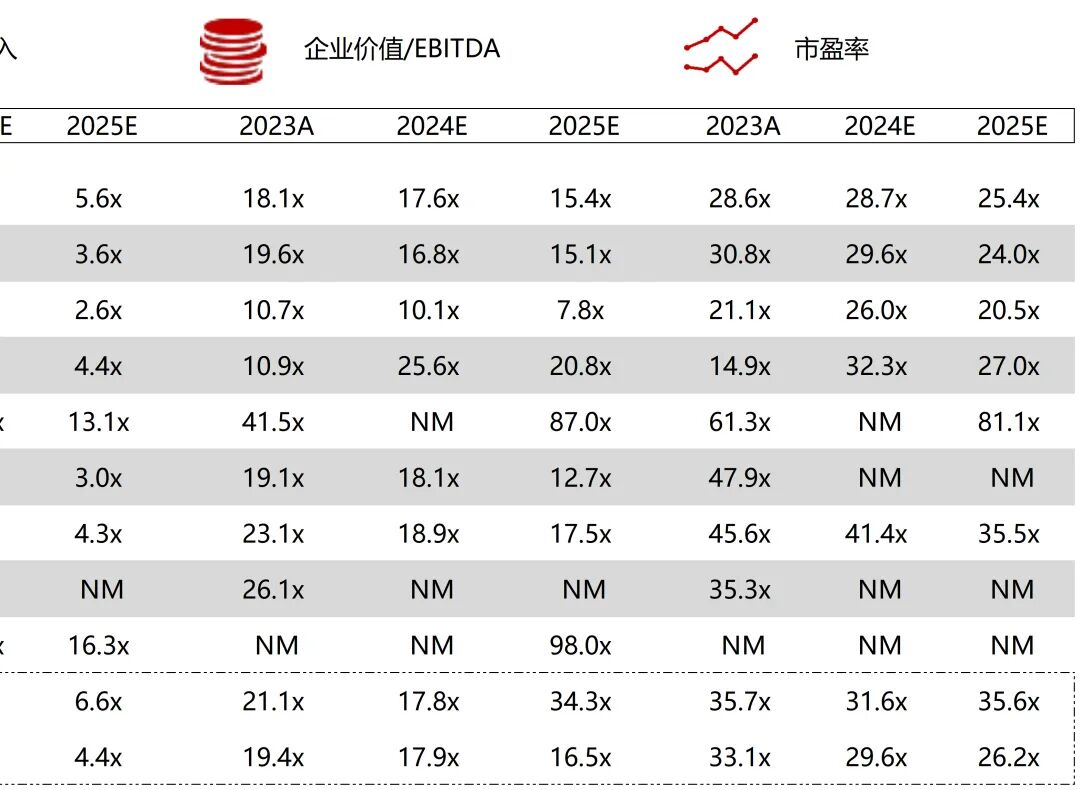
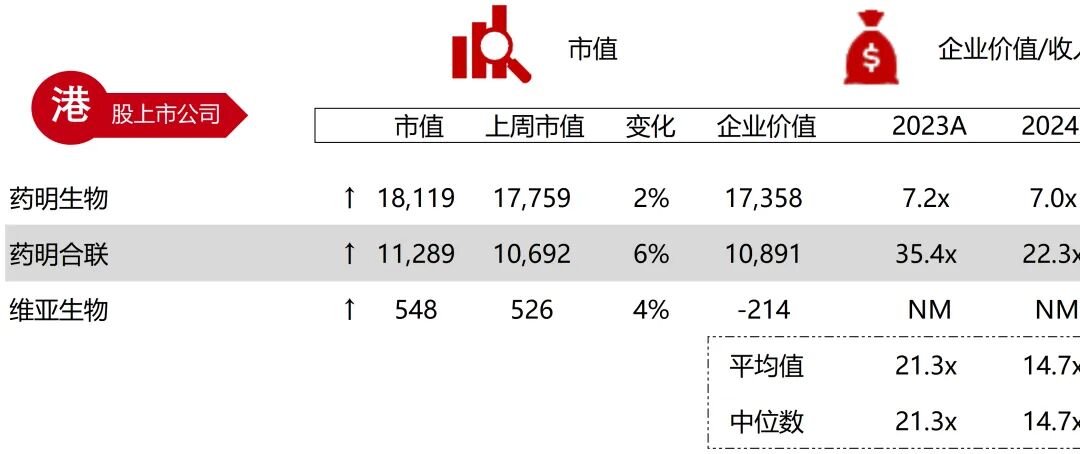
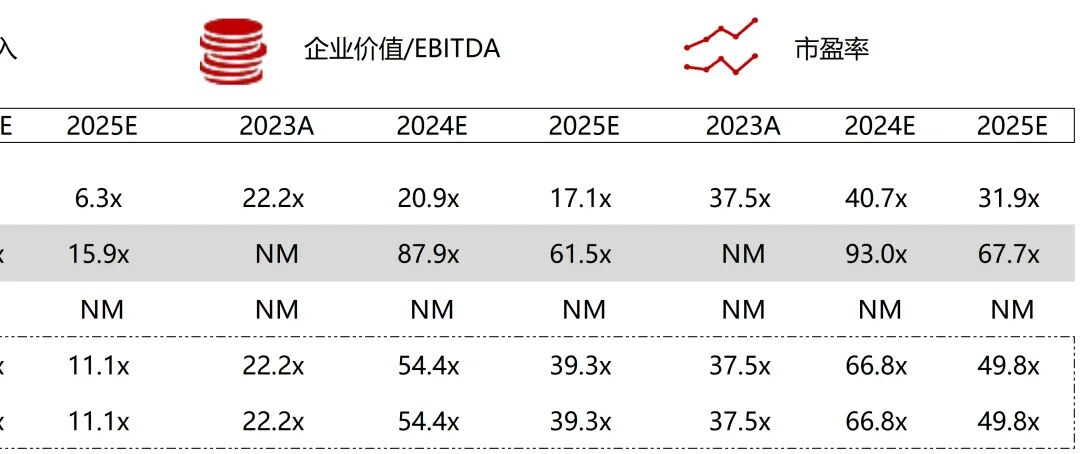
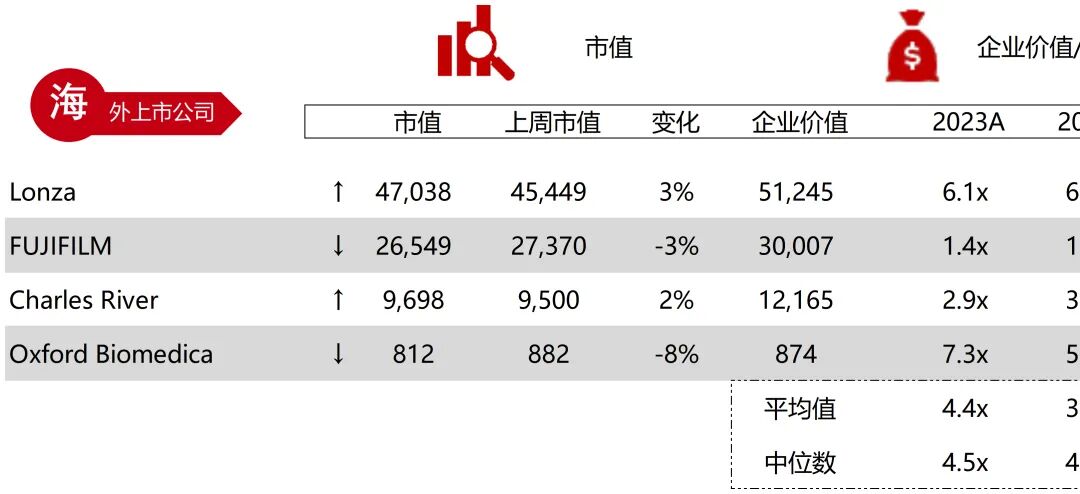
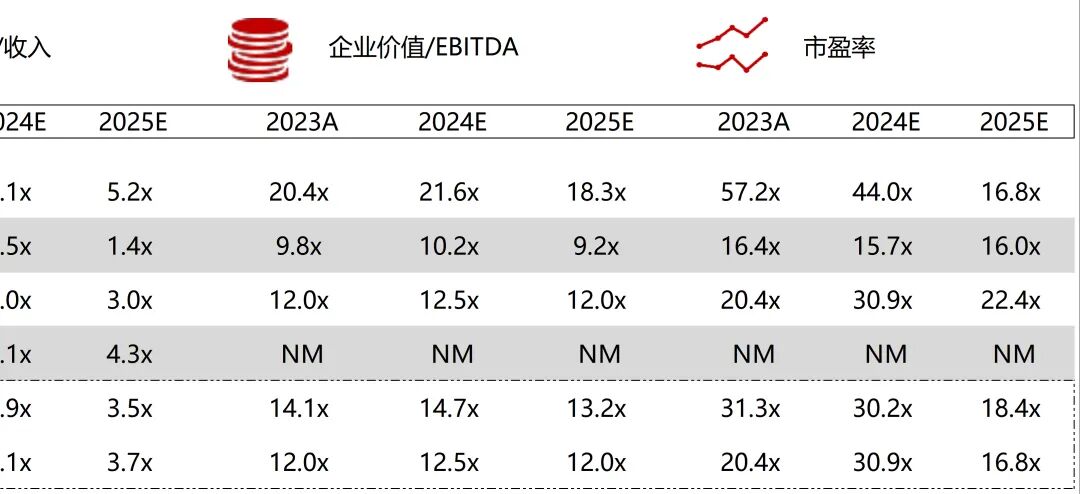
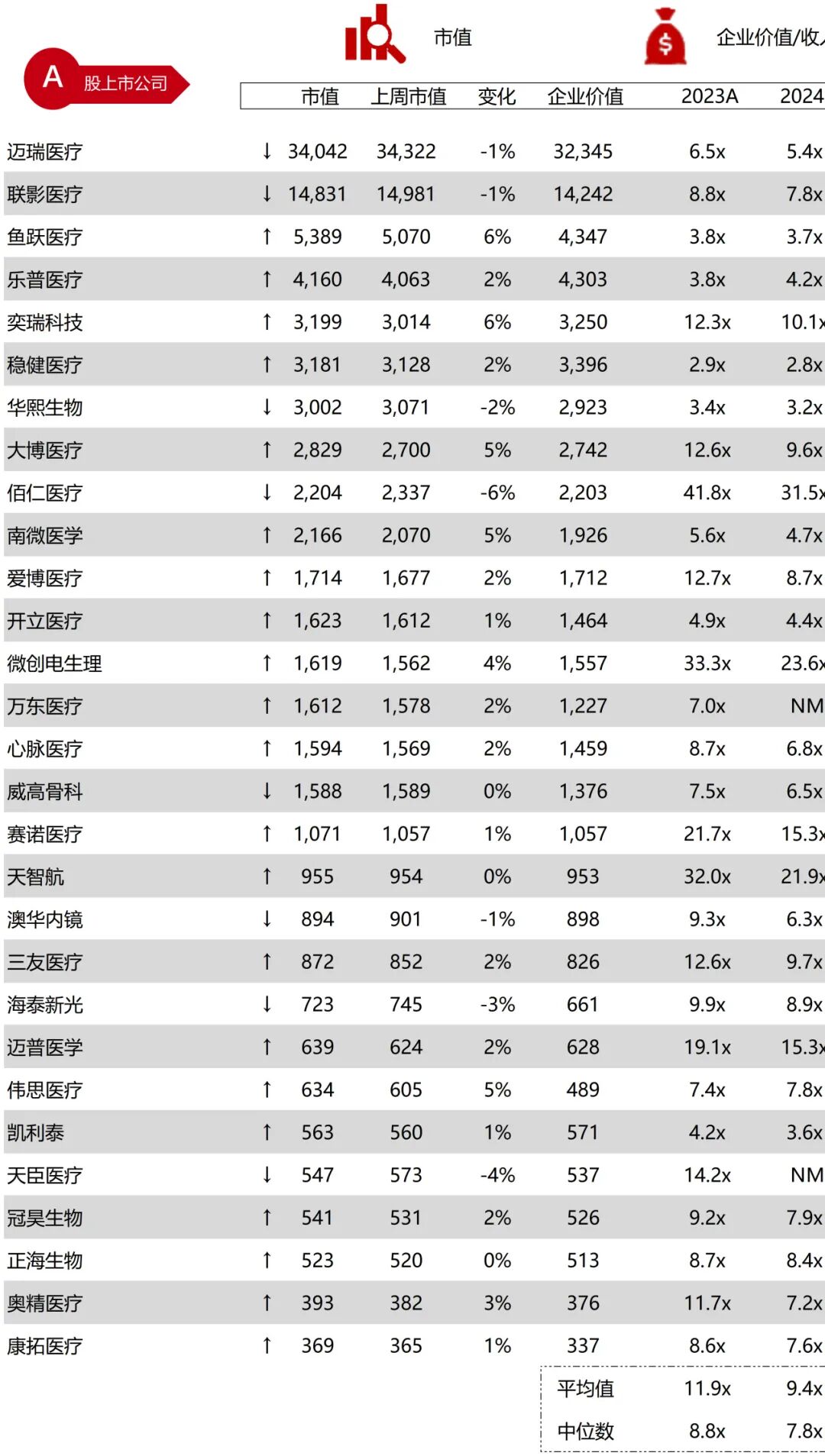
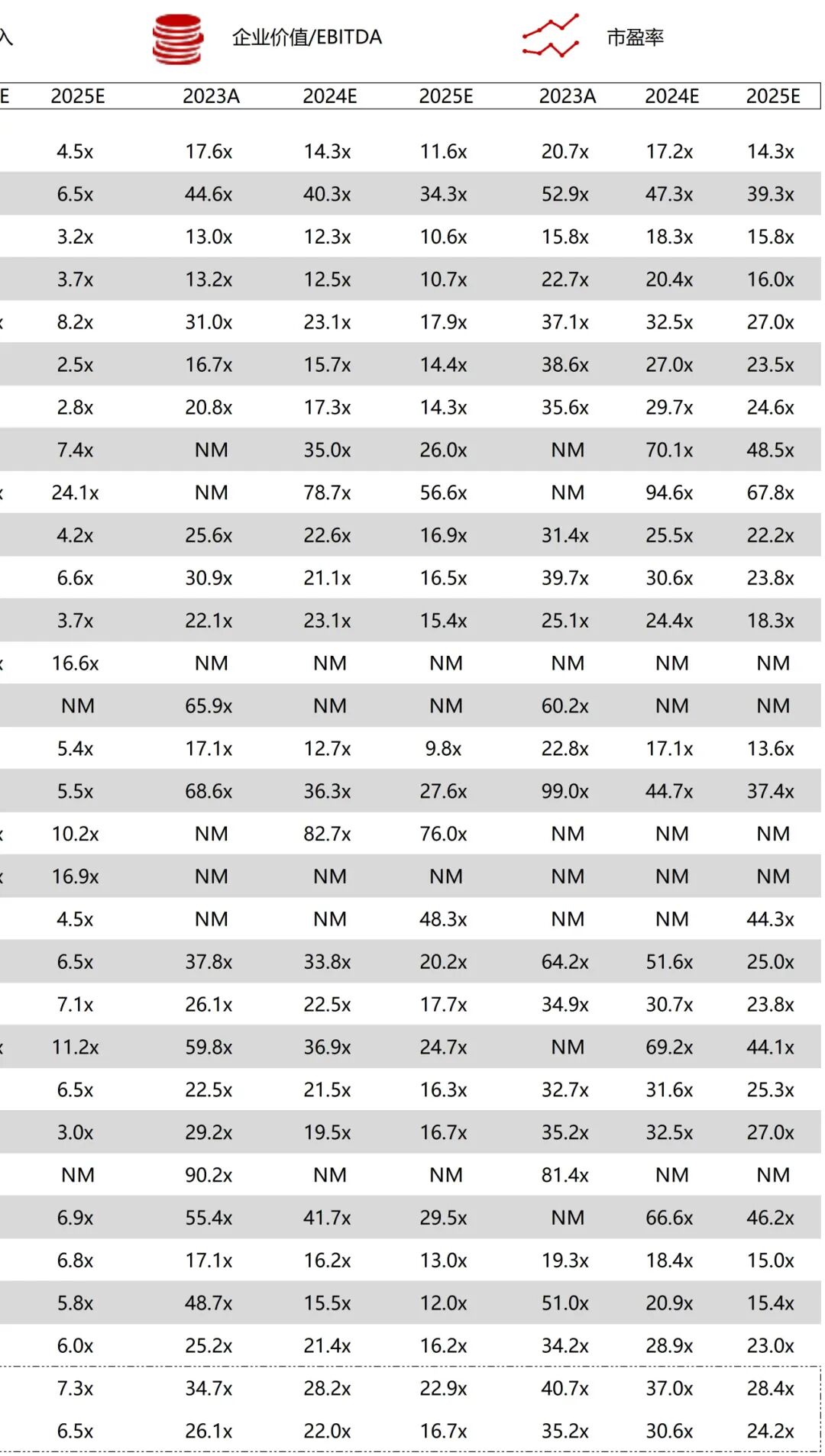
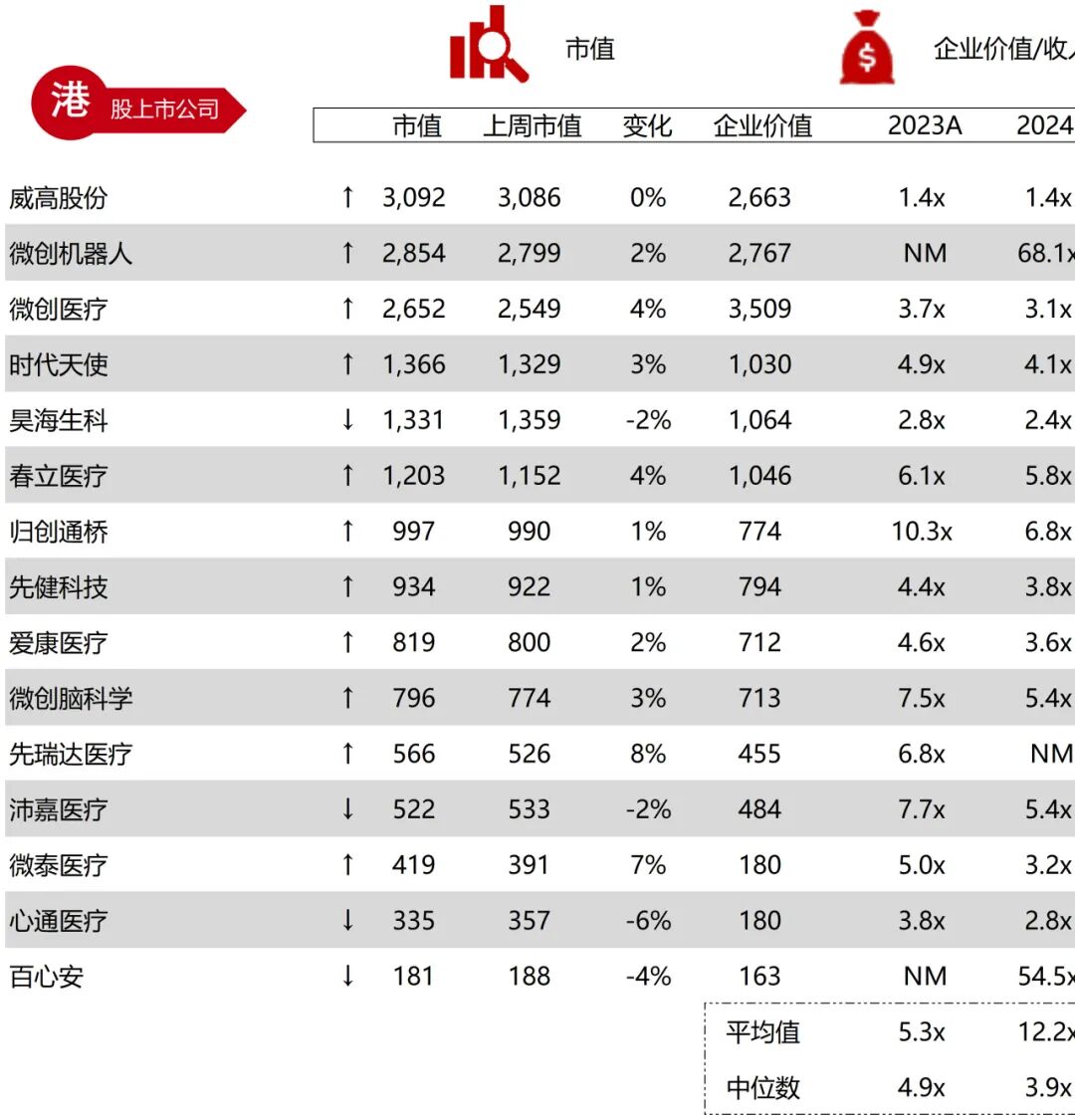
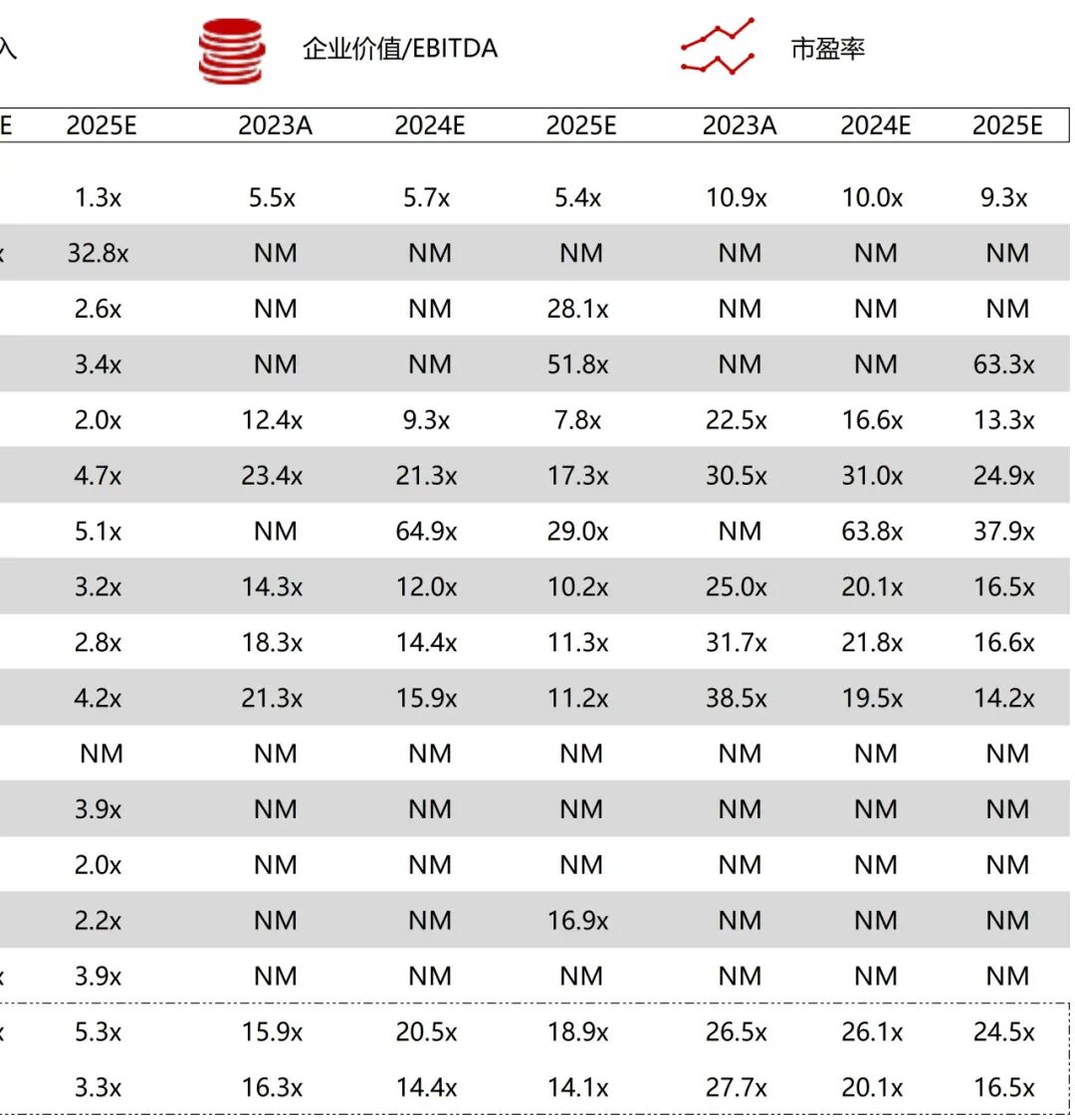
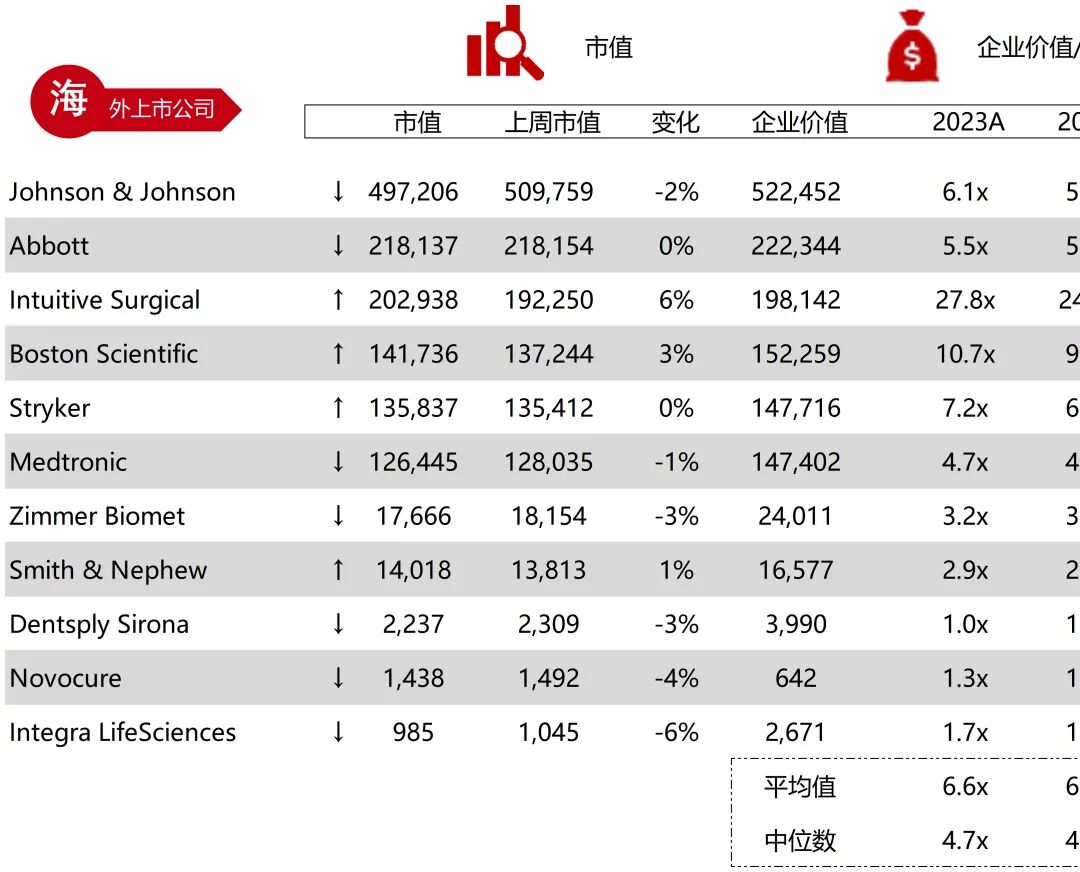
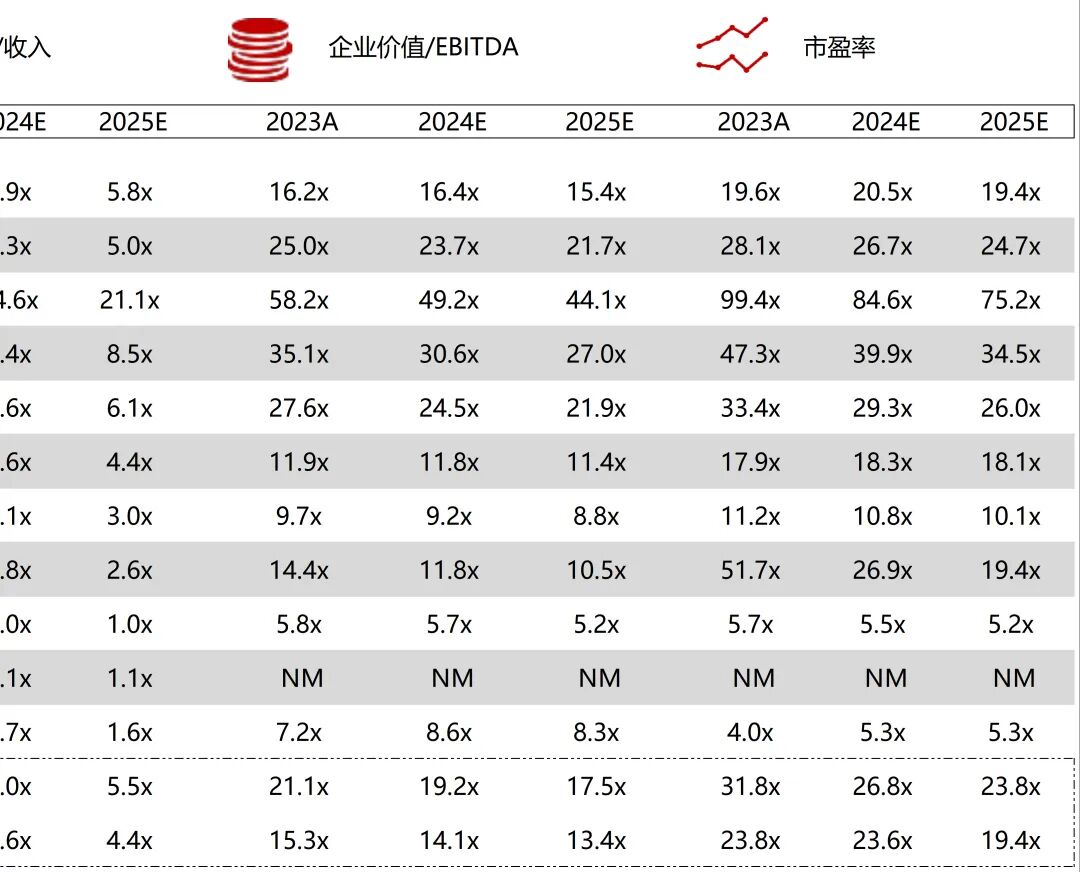
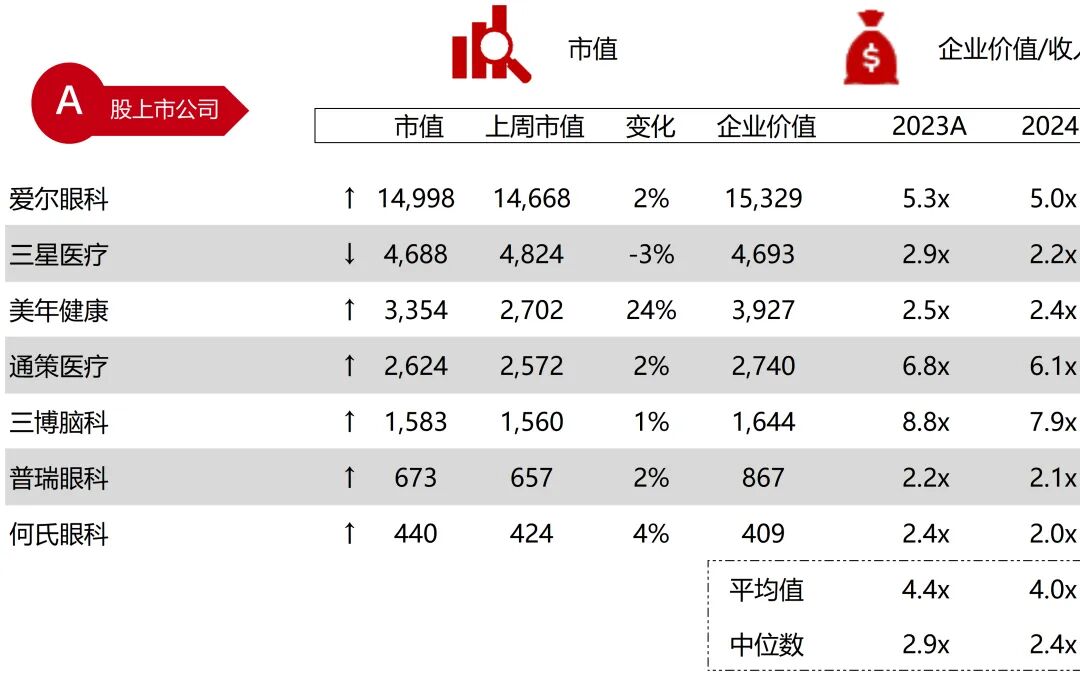
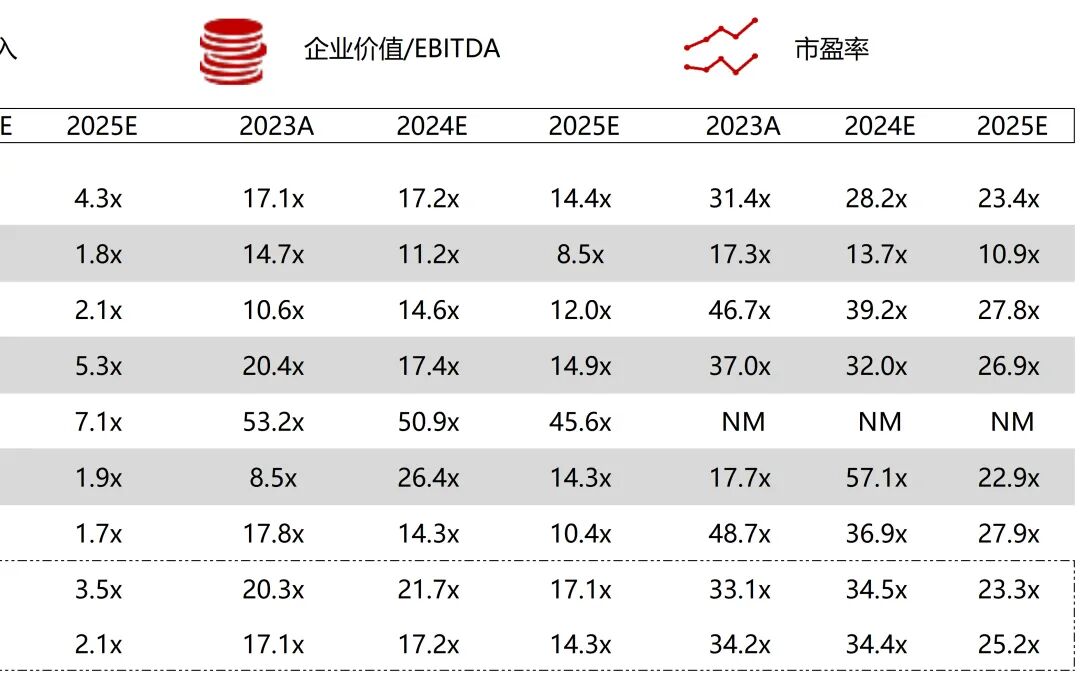
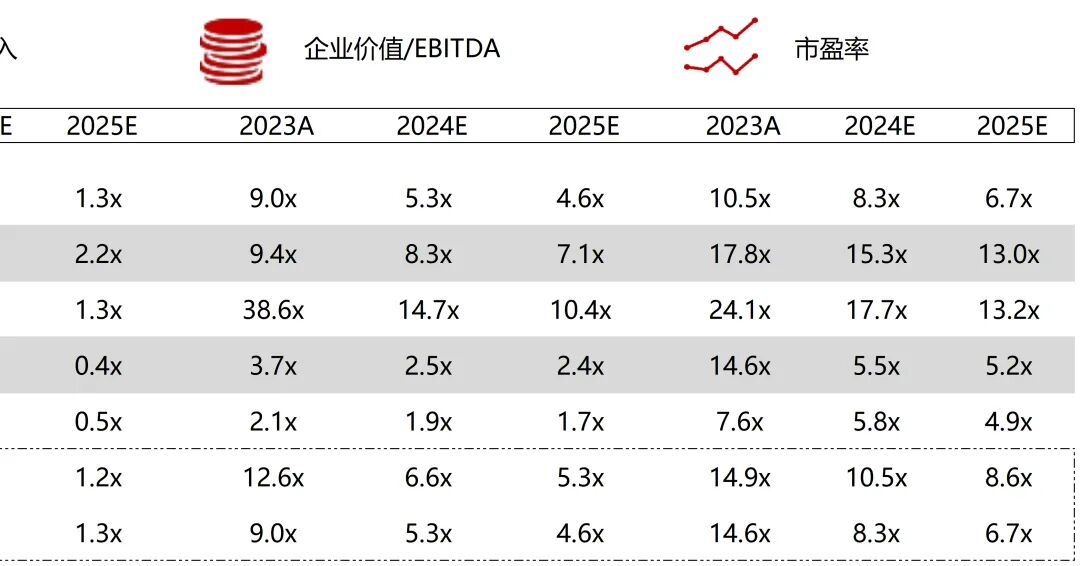
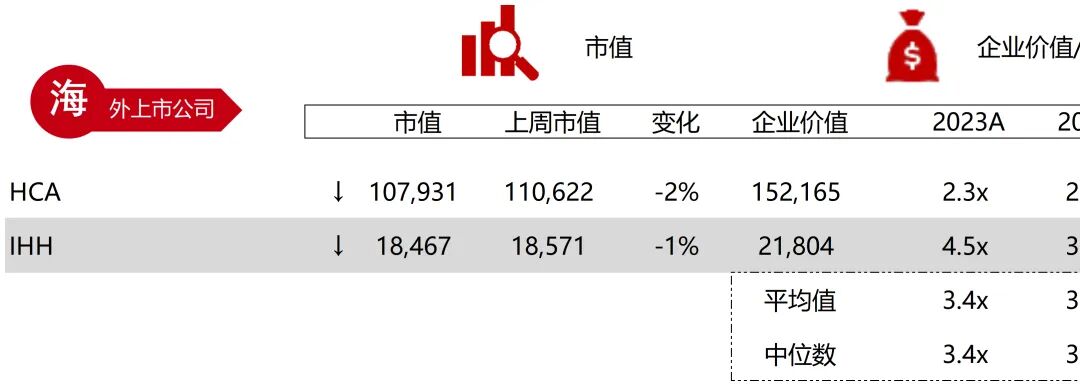
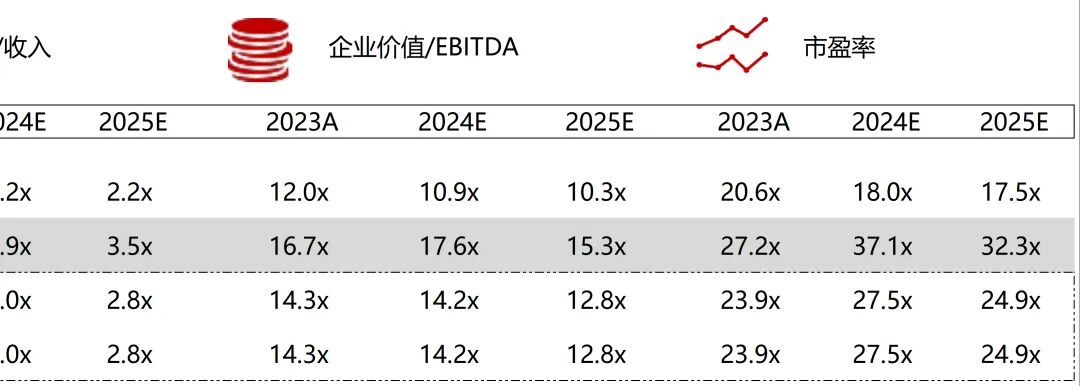
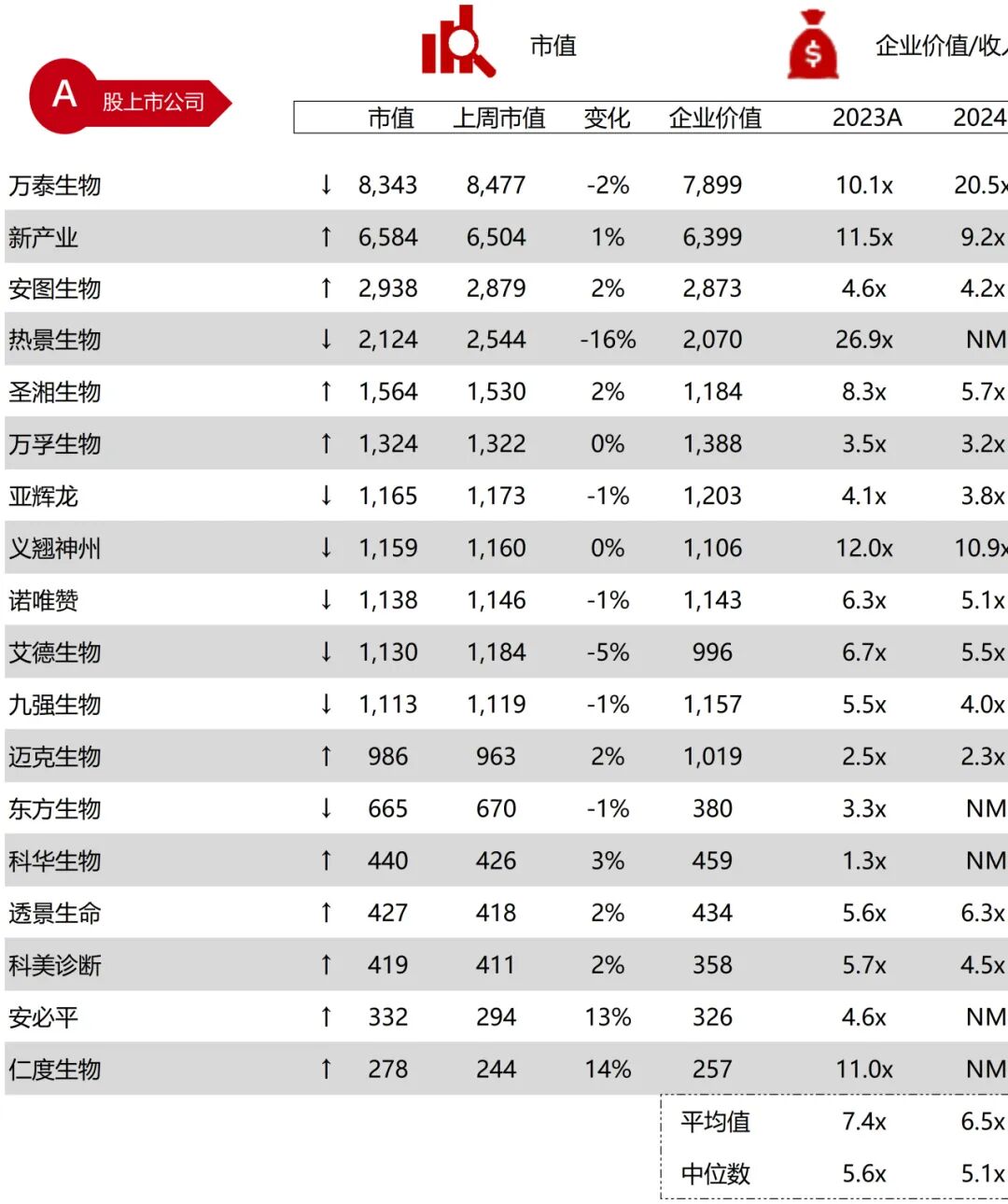
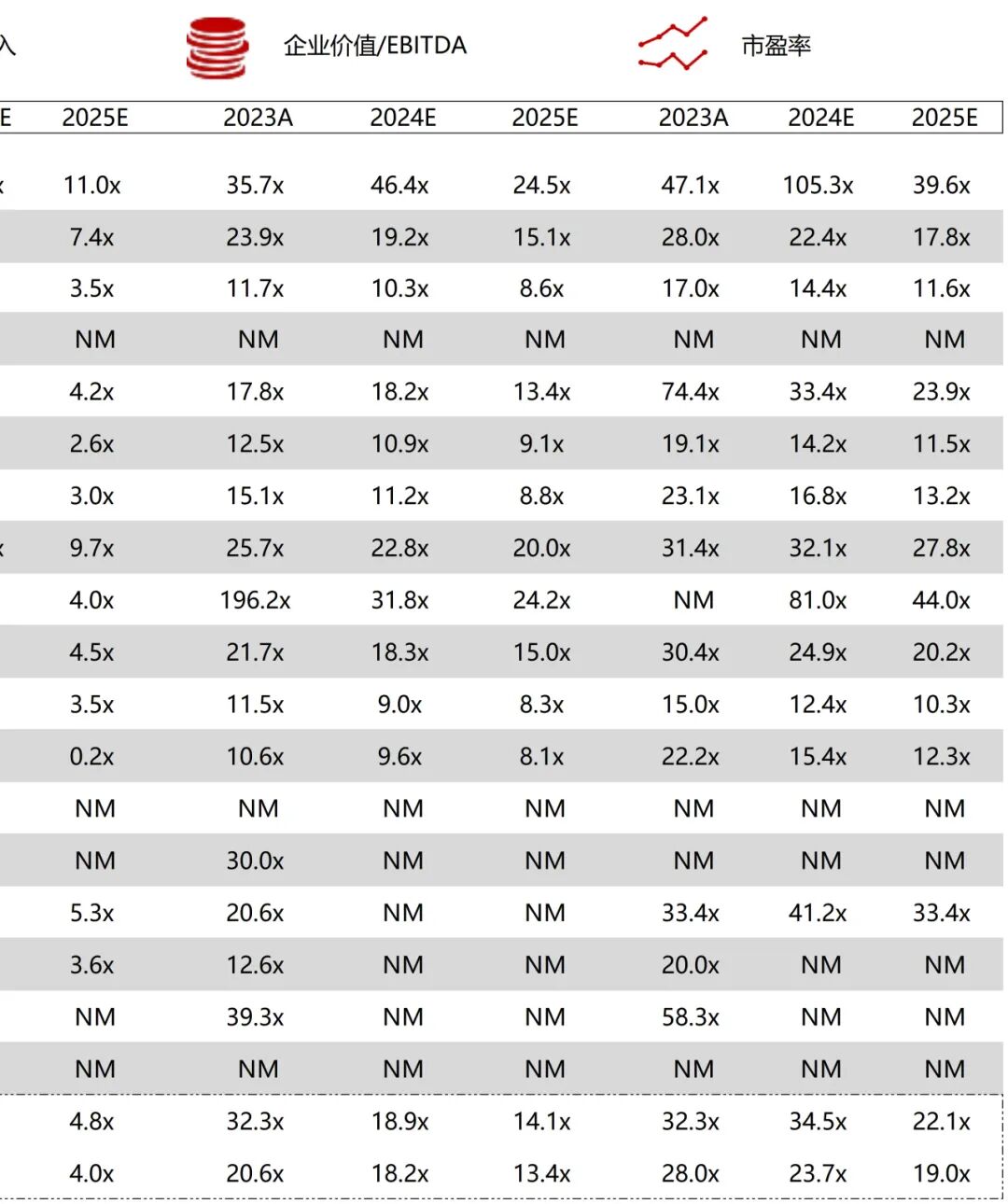
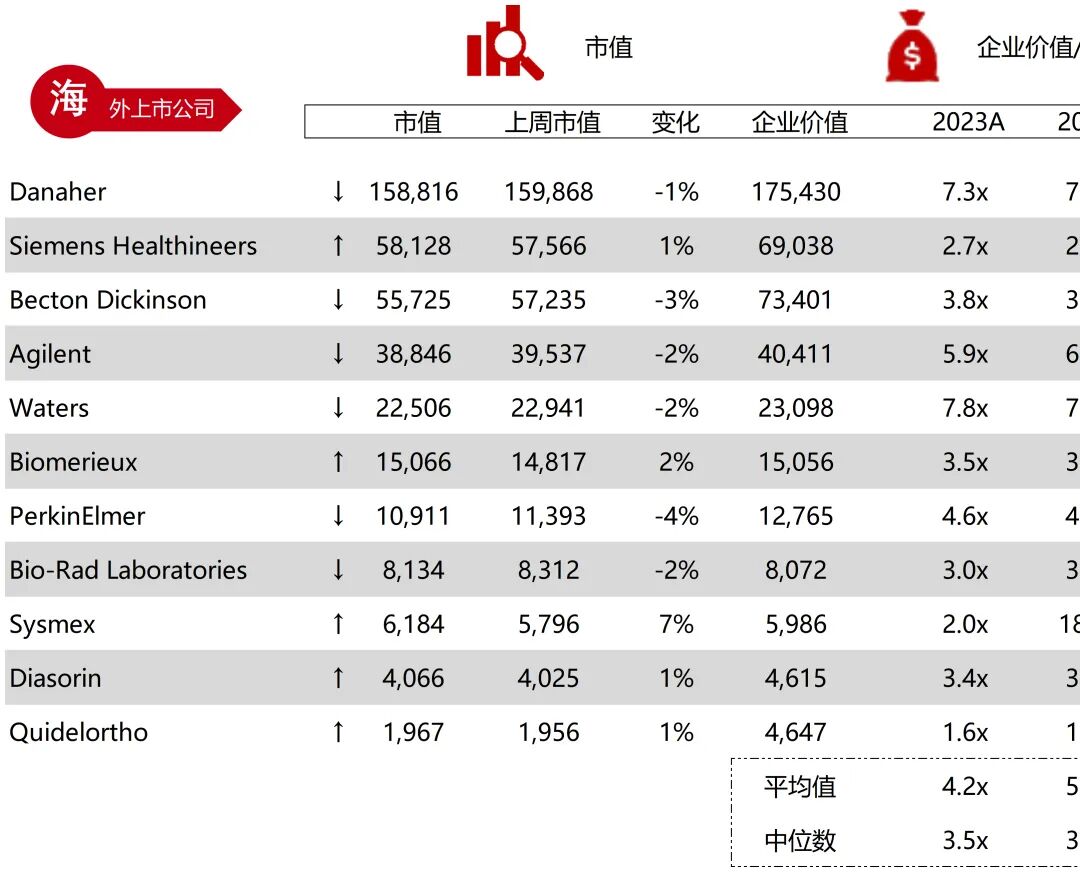
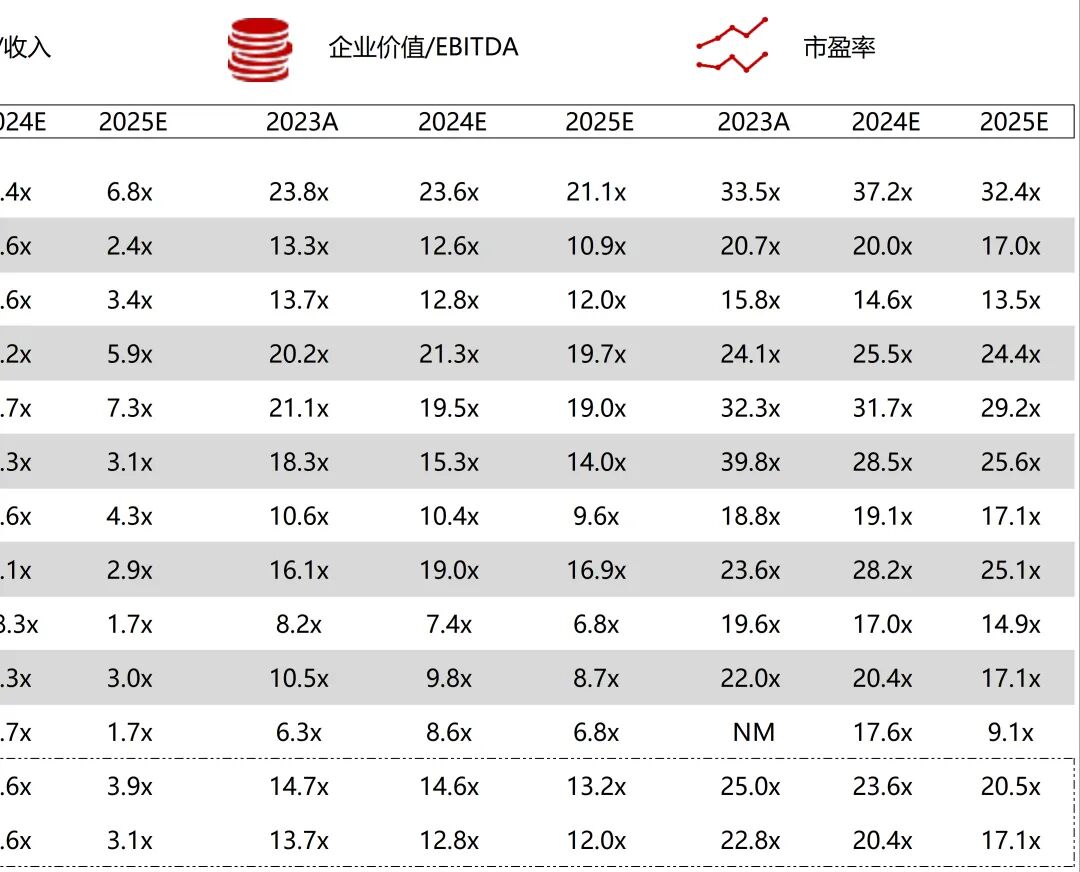
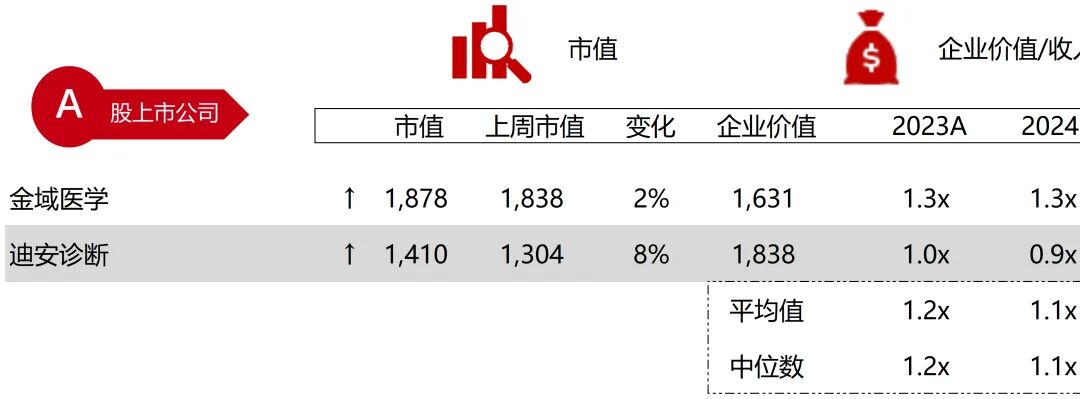
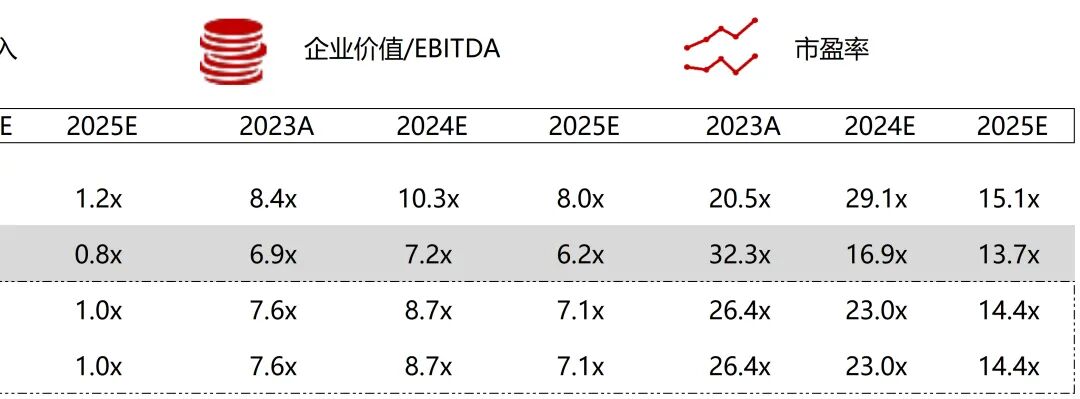
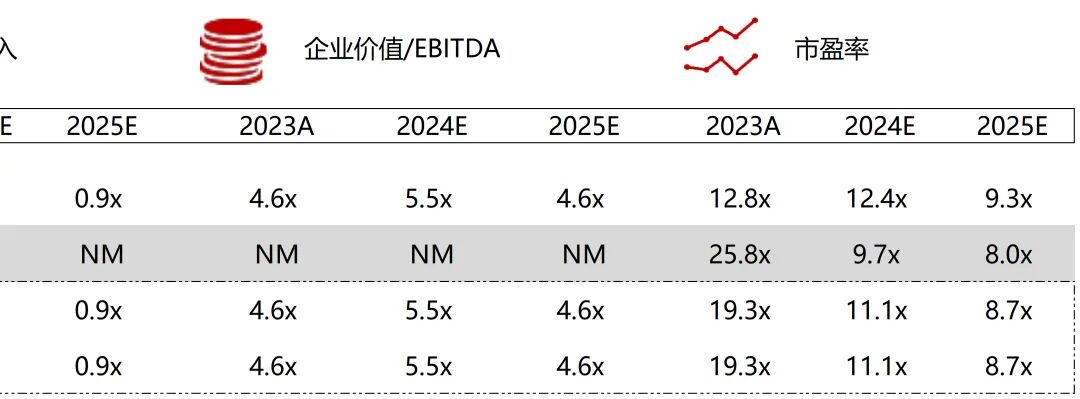
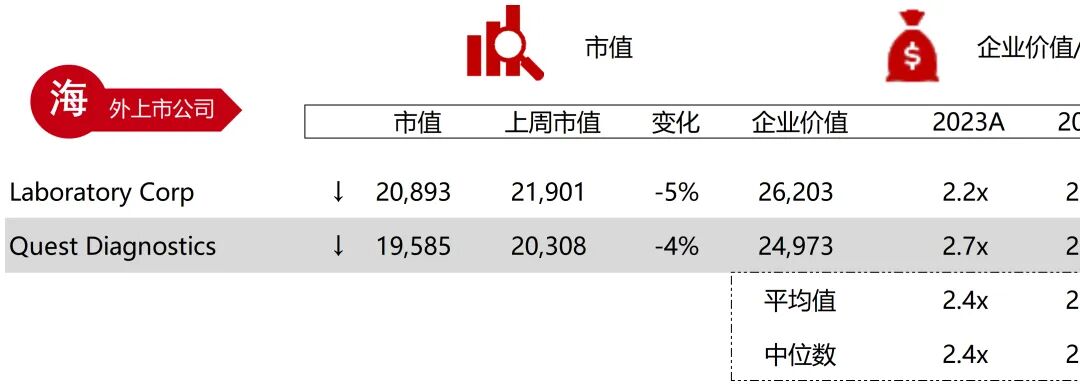
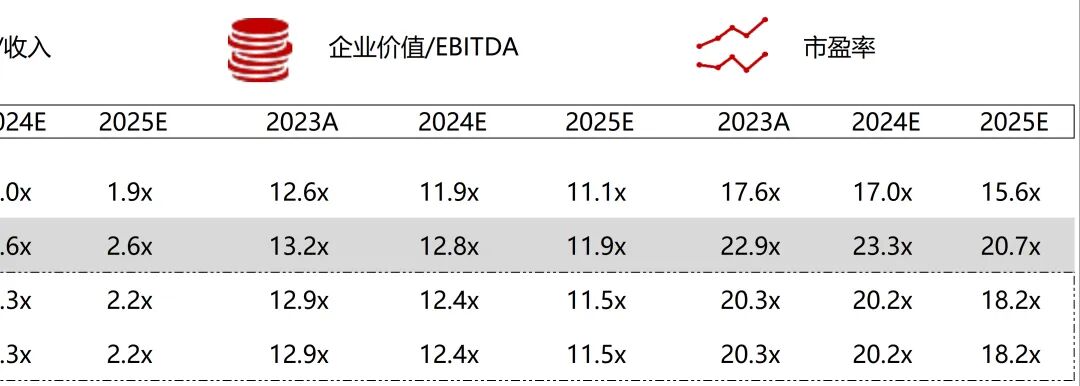
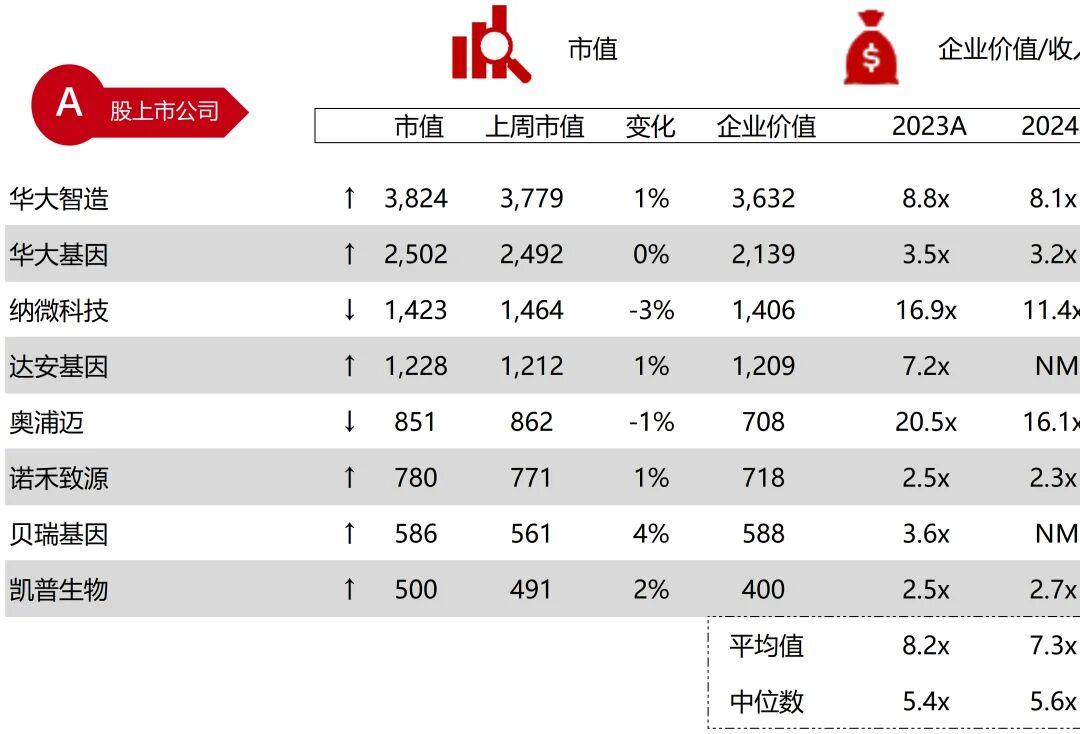
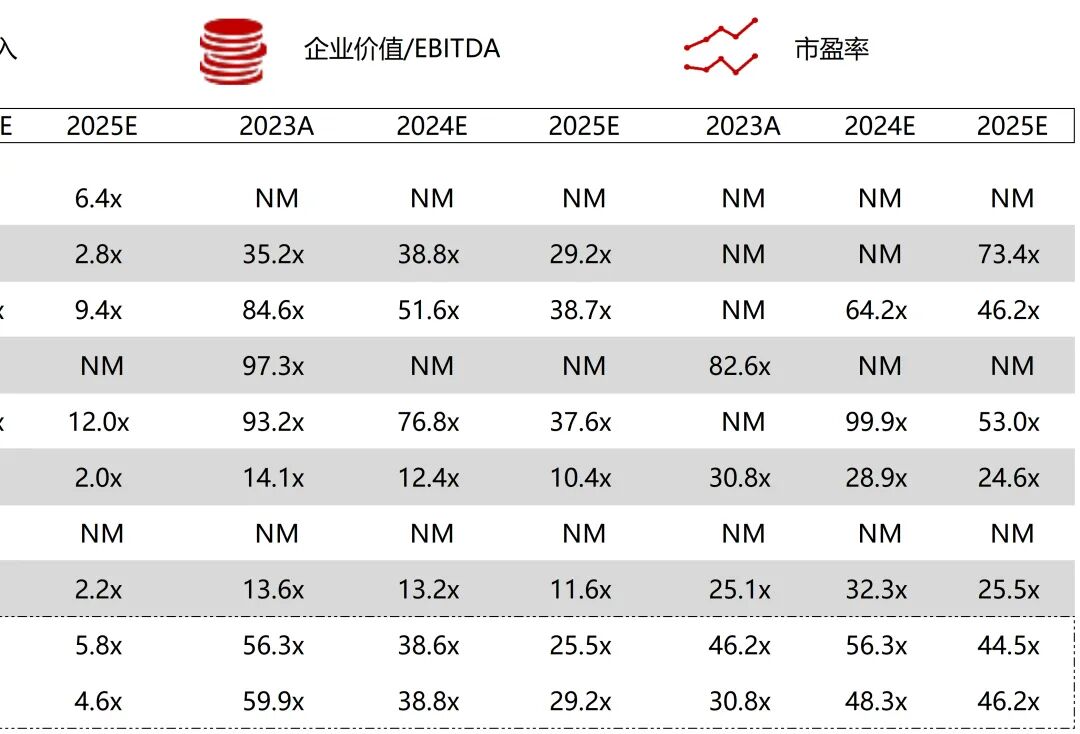
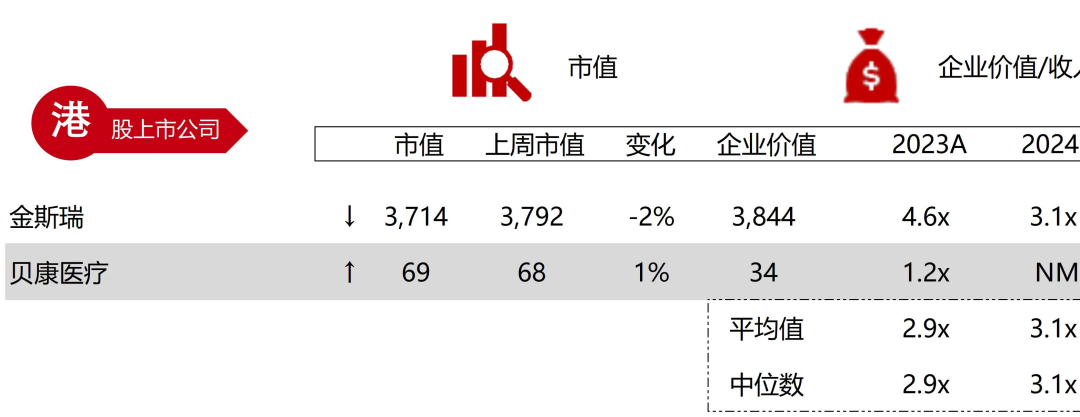
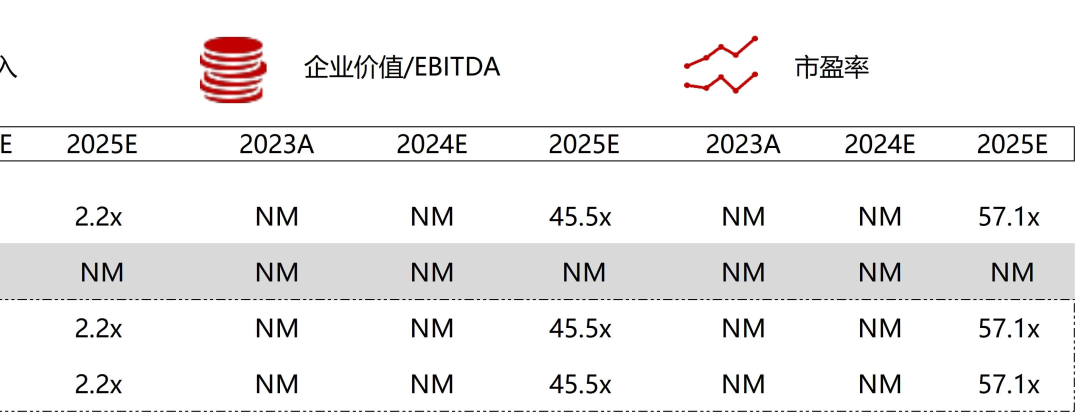
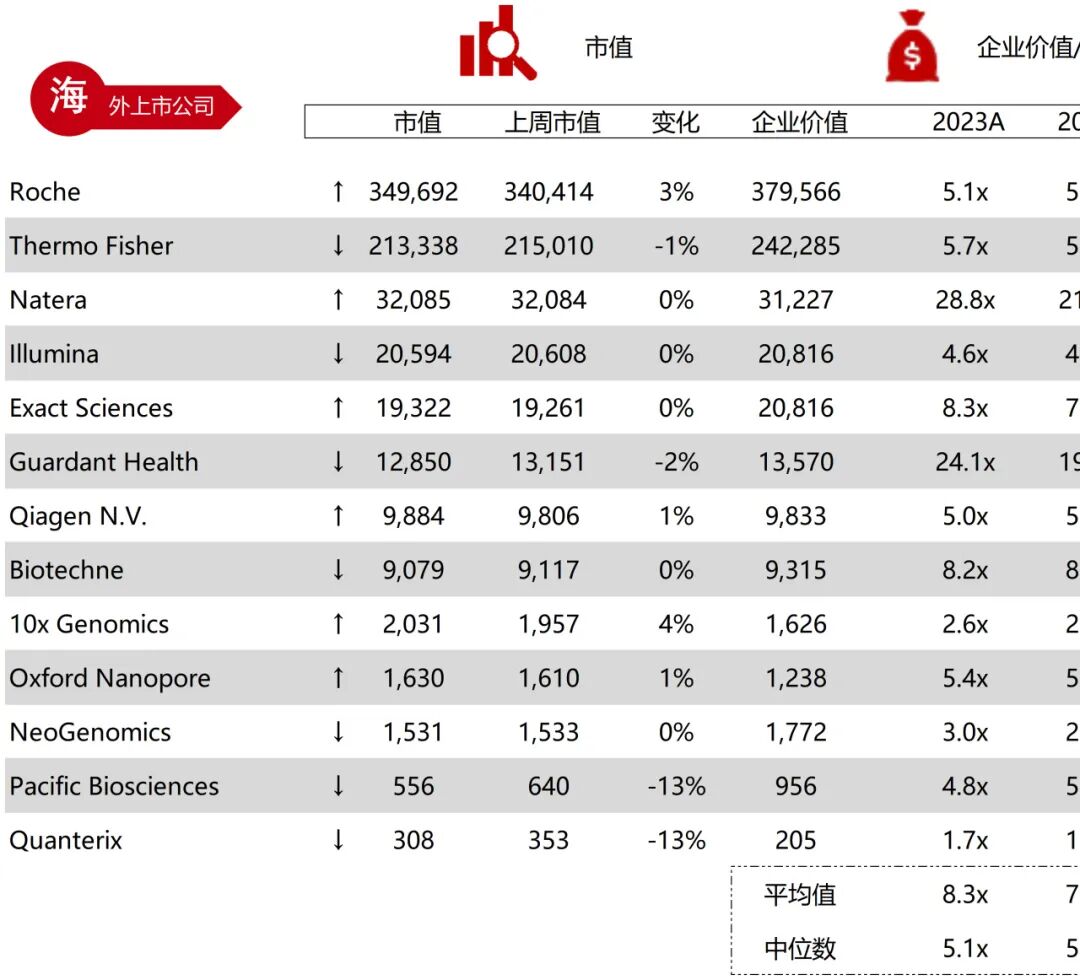
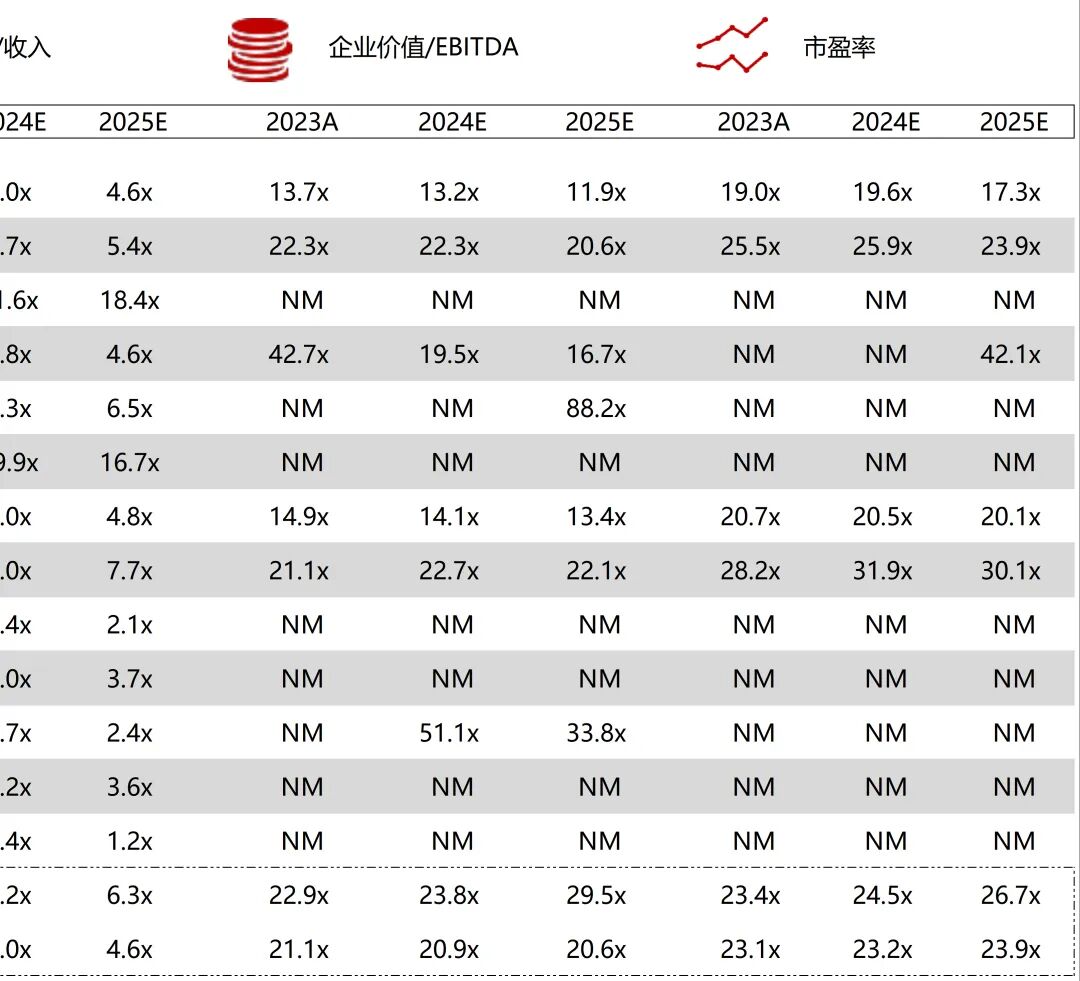
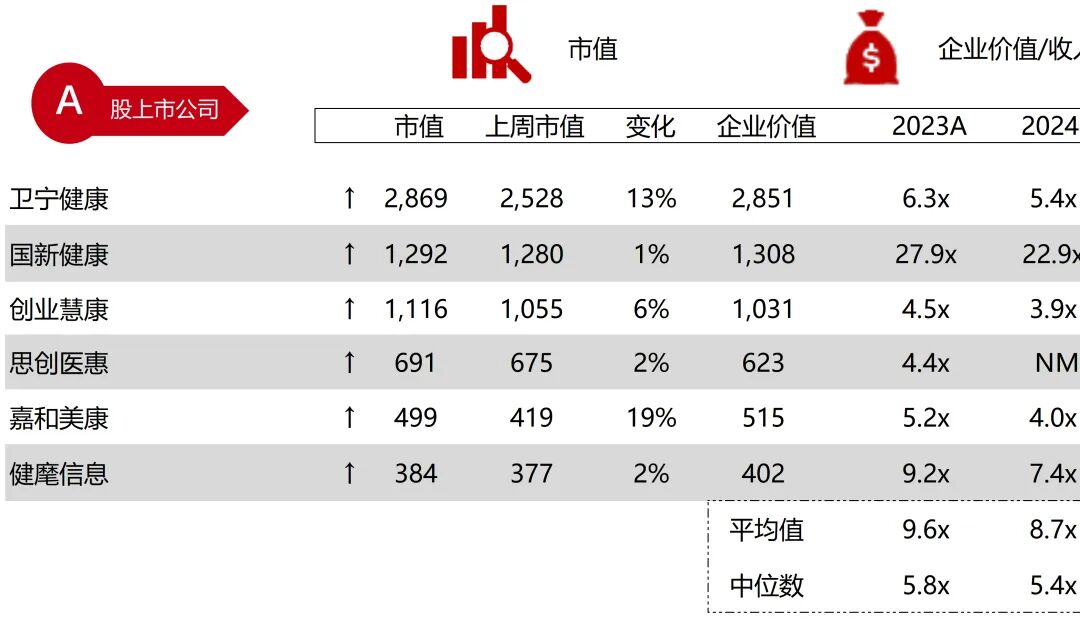
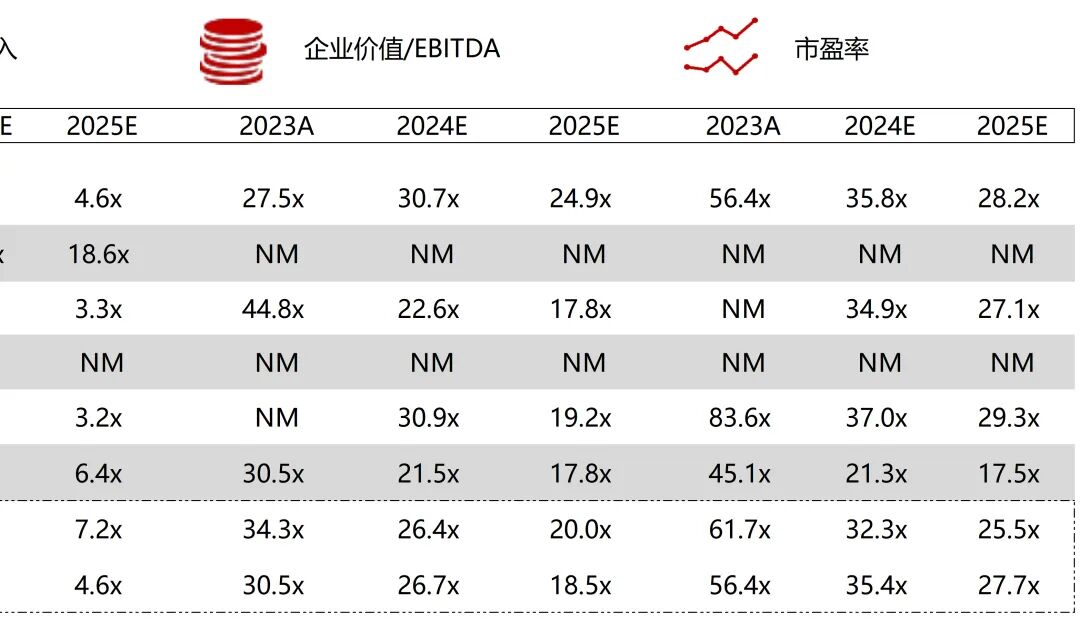
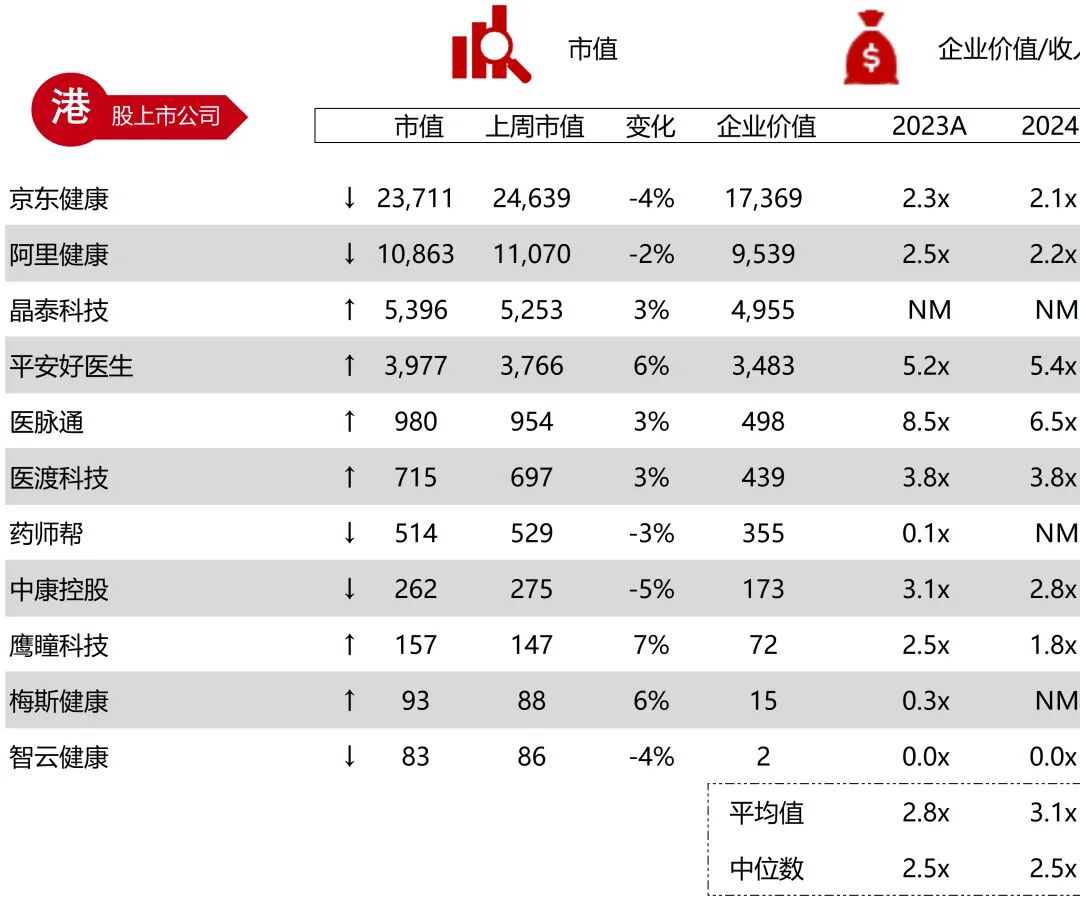
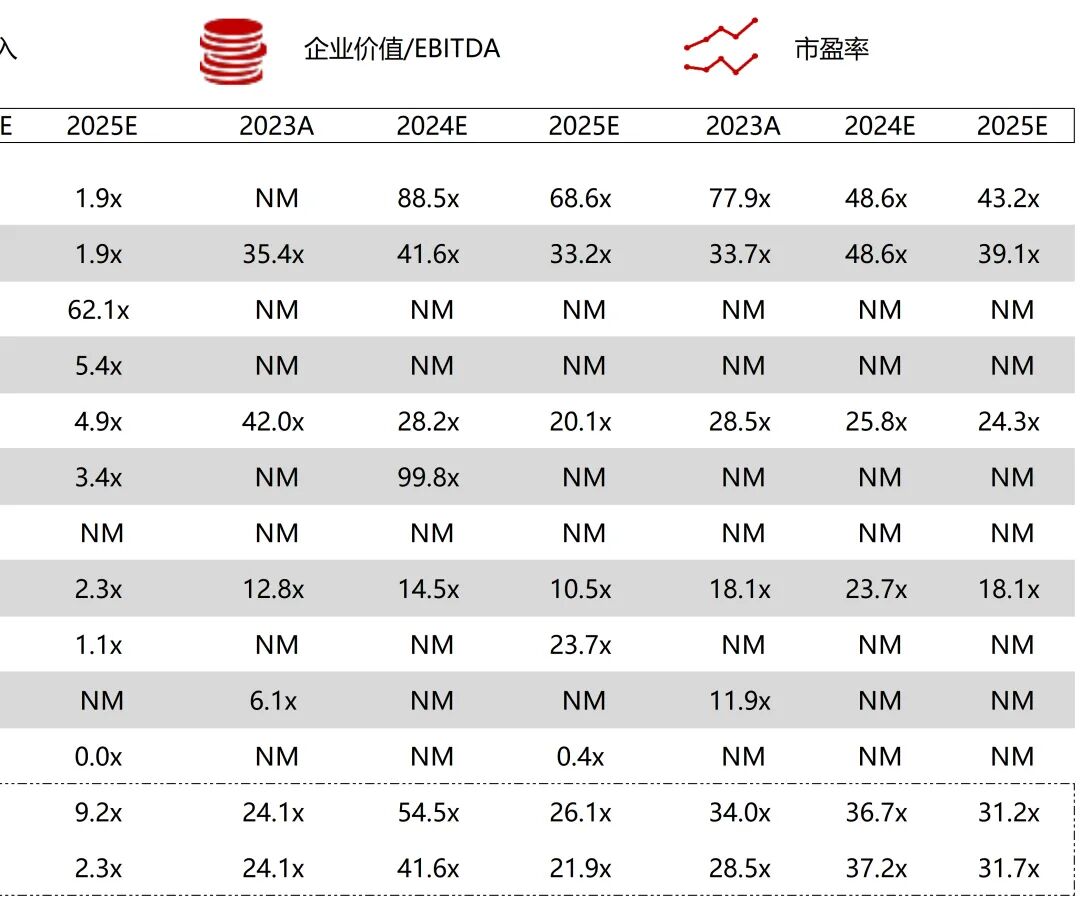
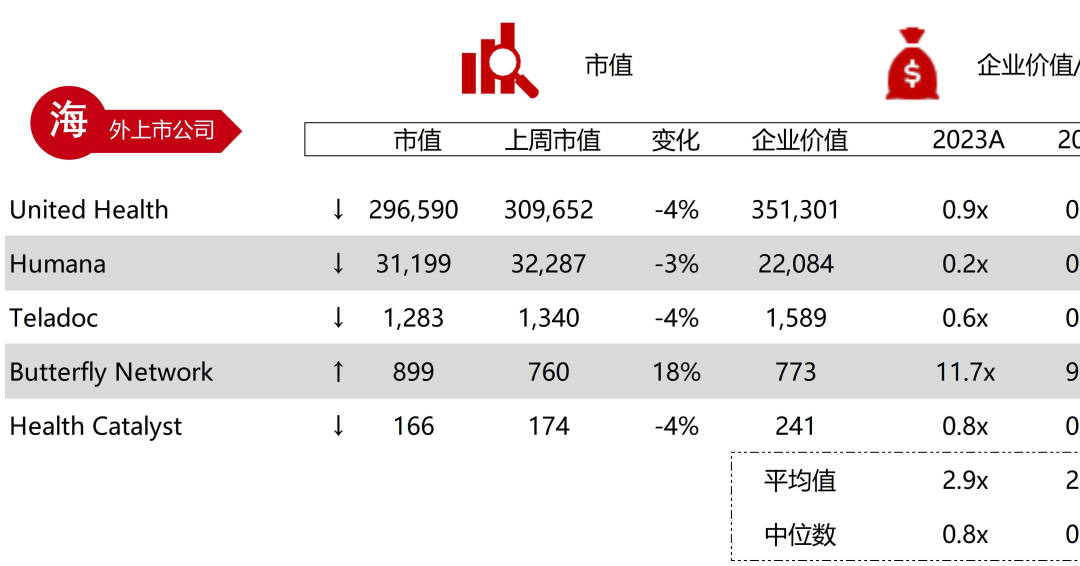
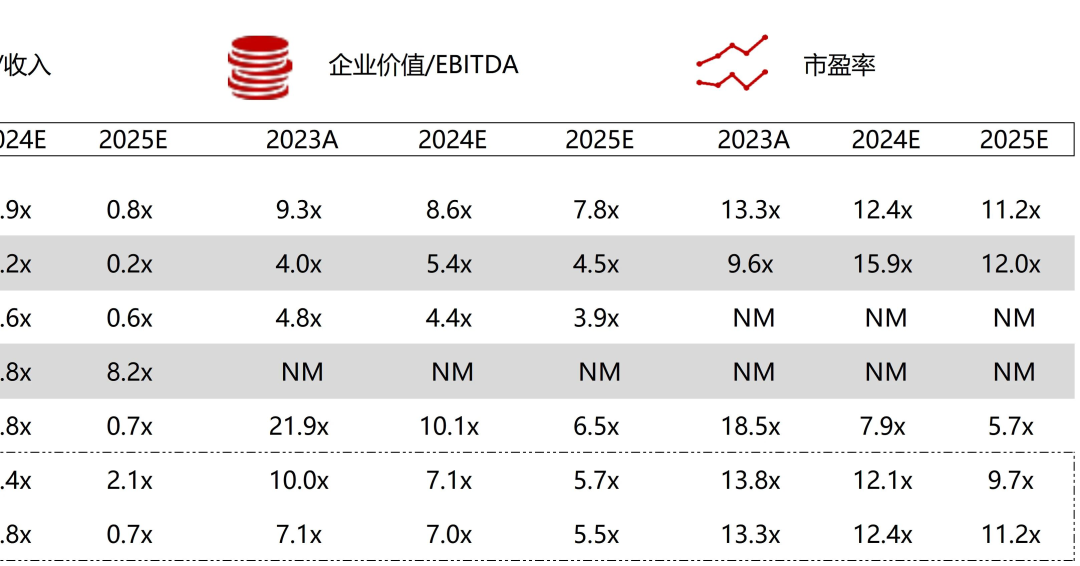
统计区间:2025年12月15日-2025年12月19日
*数据来源:华兴资本内部整理
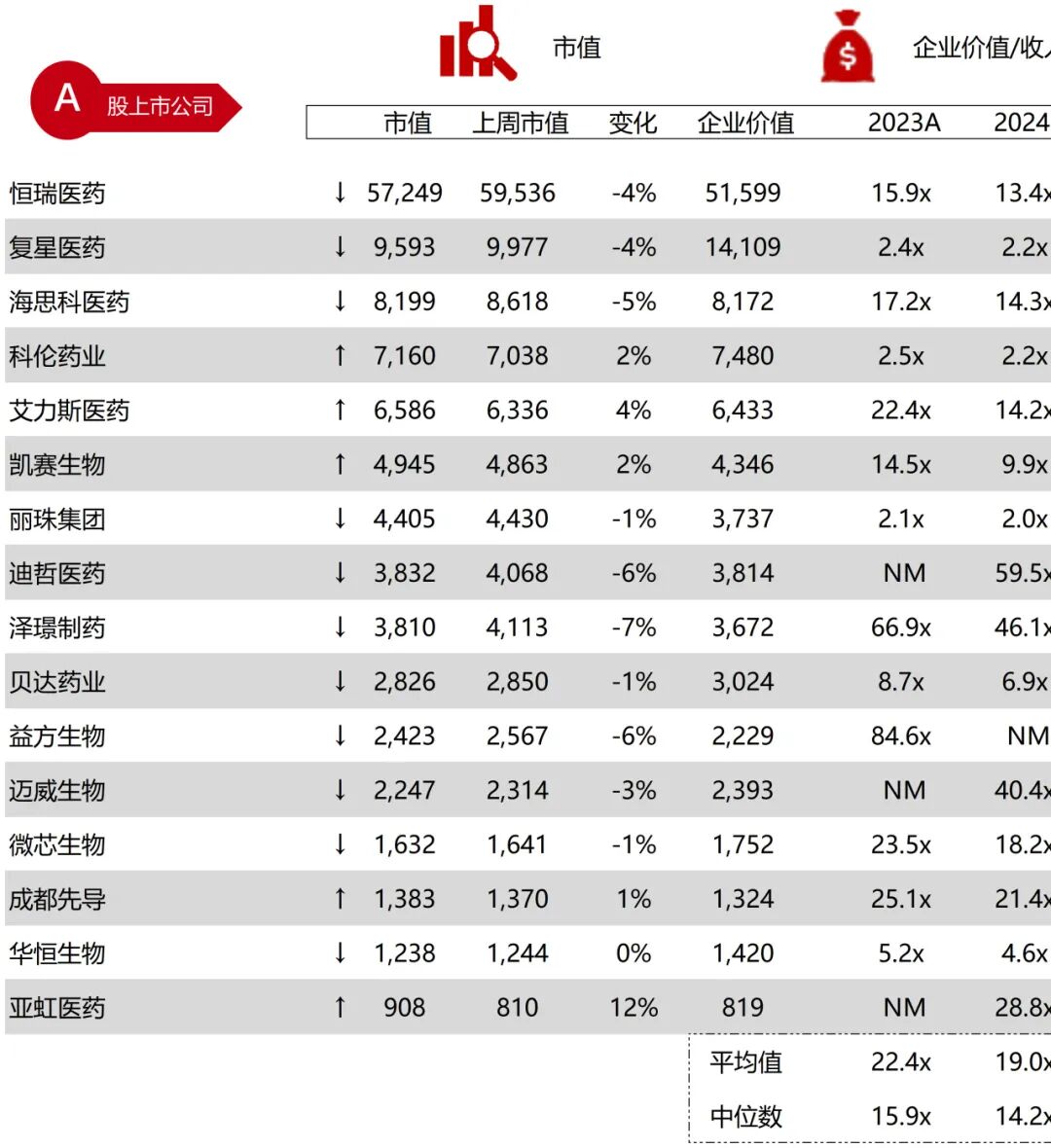
市值日期:2025年12月19日
市值单位:百万美元
*数据来源:Capital IQ、招股说明书、研报、公司年报
免责声明:本文由华兴资本集团(连同其关联公司,统称“华兴资本”)编写,谨供接收方作参考用途,并非作为也不应被视为在任何地区对任何证券的研究报告,不构成买卖、认购证券或其它金融工具及产品的邀请或保证。本文所提及的上市公司仅为示例,不代表任何投资分析或投资建议。接收方不应仅依靠本文,而应按照自己的判断作出投资决定,并在作出任何投资行动前,咨询专业意见。
本文所载资料的来源皆被华兴资本认为可靠,但华兴资本概不担保本文所含信息的准确性、完整性或新近度。本文所载的见解、分析、预测、推断和期望均截至本文的发表日期,且可能在未经事先通知的情况下调整。华兴资本与本文所提及的公司之间可能存在或寻求业务关系,因此,接收方请知悉可能存在的影响本文客观性的利益冲突。华兴资本不对因使用本文而承受的直接或间接损失承担任何责任。本文受到版权和资料全面保护。







































精彩评论