成都恩沐生物于2021年12月22日收到美国FDA的SMP(Study May Proceed)信函,靶向CD3、CD19和CD20的三特异抗体1A46用于治疗难治、复发B细胞恶性血液肿瘤的临床试验申请获得FDA正式批准。
时隔一周,12月29日中国临床试验申请也获得批准。
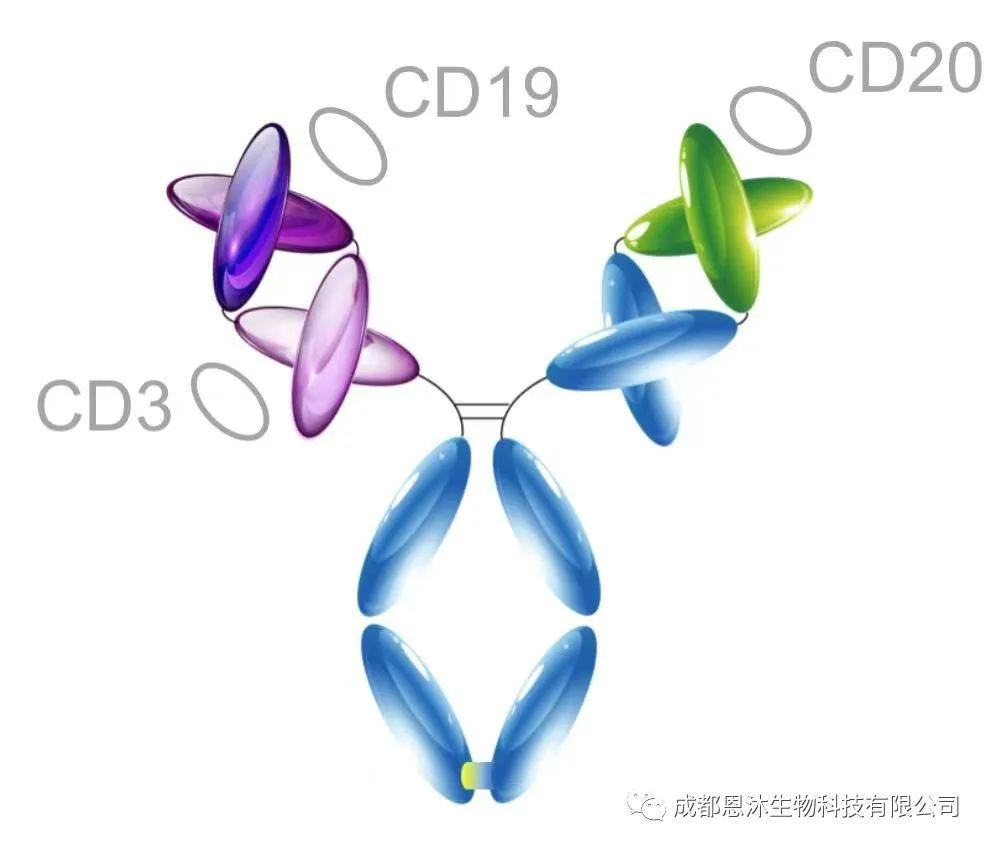
这是全球首个进入临床研究的CD3/CD19/CD20的三靶点抗体新药,同时也是中国第一个获得美国FDA批准临床的靶向CD3的T细胞介导型抗体(T-cell engager)。
恩沐生物计划于8家医院开展临床研究,由MD Anderson癌症研究中心的两位著名专家分别担任B-ALL和B-NHL研究的leading PI。而大中华地区权益近期已授权海正博锐生物。
五年前,创新药大潮初起,成都高投创投的张继说服周桢昊创业成立恩沐生物,并说服了张洁加入创始团队。
在中国做创新药已属不易,做全球前沿的双特异、三特异抗体研发平台更是难上加难,现在公司全球1A46项目获得NMPA和FDA临床试验许可,表明多特异抗体生物药的临床前研发水平及质量已得到中美药监部门的肯定。研发管线也储备有十余个双特异/三特异抗体分子,针对不同适应症。
一路走来,筚路蓝缕,披荆斩棘,受风霜劳累之苦,多难兴业。此时晨曦微露,让人更起奋勇前进之心。
精彩评论