2025年5月14日,由AbbVie研发的一款靶向c-Met ADC药物Telisotuzumab vedotin(Teliso-V, 商品名Emrelis) 获得了美国食品药品监督管理局(FDA)的加速批准上市,用于既往接受过全身治疗的局部晚期或转移性、高c-Met蛋白表达的非小细胞肺癌(NSCLC)成人患者的治疗。Teliso-V是全球首款且唯一获批上市的c-Met靶向ADC药物,同时也是首个专门针对c-Met高表达NSCLC患者的first-in-class疗法。这个历经小分子药物和双抗验证的“老靶点”,正借助ADC技术焕发新生。
本文从c-Met靶点、c-Met ADC开发进展、BD交易、竞争格局等多个维度进行分析,旨在为读者提供c-Met靶向ADC治疗领域的洞察与战略启示。
c-Met靶点:癌症治疗领域的“老树新芽”
c-Met 该靶点自 1984 年被发现以来,经历了三个发展历程,近年来,由于基础科研和临床研究的诸多新的进展和发现让c-Met靶向药物的研发重新吸引了市场目光。
第一阶段:小分子抑制剂
例如,诺华的Capmatinib、默克的Tepotinib及阿斯利康/和黄医药的Savolitinib靶向 MET突变型NSCLC,尽管疗效确切且开发较早,但小分子抑制剂往往存在特定突变类型限制,耐药和毒性问题,促使目光转向新的技术平台。
第二阶段:双抗
强生推出的EGFR/c-Met双抗Amivantamab,突破了依赖基因突变筛选的传统模式。其通过双靶点协同阻断,显著提升治疗获益,在一线治疗中将疾病进展风险降低30%。
第三阶段:ADC
艾伯维首次将ADC技术成功引入c-Met高表达肿瘤治疗领域。在Teliso-V 的II期临床数据显示,总体人群、c-Met高表达和c-Met中等表达患者的客观缓解率(ORR)分别为28.6%、34.6%和22.9%,中位总生存期(OS)分别为14.5个月、14.6个月和14.2个月,充分展现了ADC技术在c-Met治疗上的独特优势。
全球c-Met ADC药物研发与合作动态
据医药魔方数据统计,截至2025年7月28日,在研的c-Met ADC药物共69个,处于临床阶段的c-Met ADC药物达19个,1款药物获批上市(艾伯维的Teliso-V),如下表所示。据Beacon数据库统计,随着艾伯维Teliso-V的获批上市和国内外药企的持续创新,相较于去年,围绕c-Met ADC的临床前管线数量快速增长,一跃成为临床前试验数量的前TOP 5靶点。
全球已进入临床c-Met ADC药物研发进展
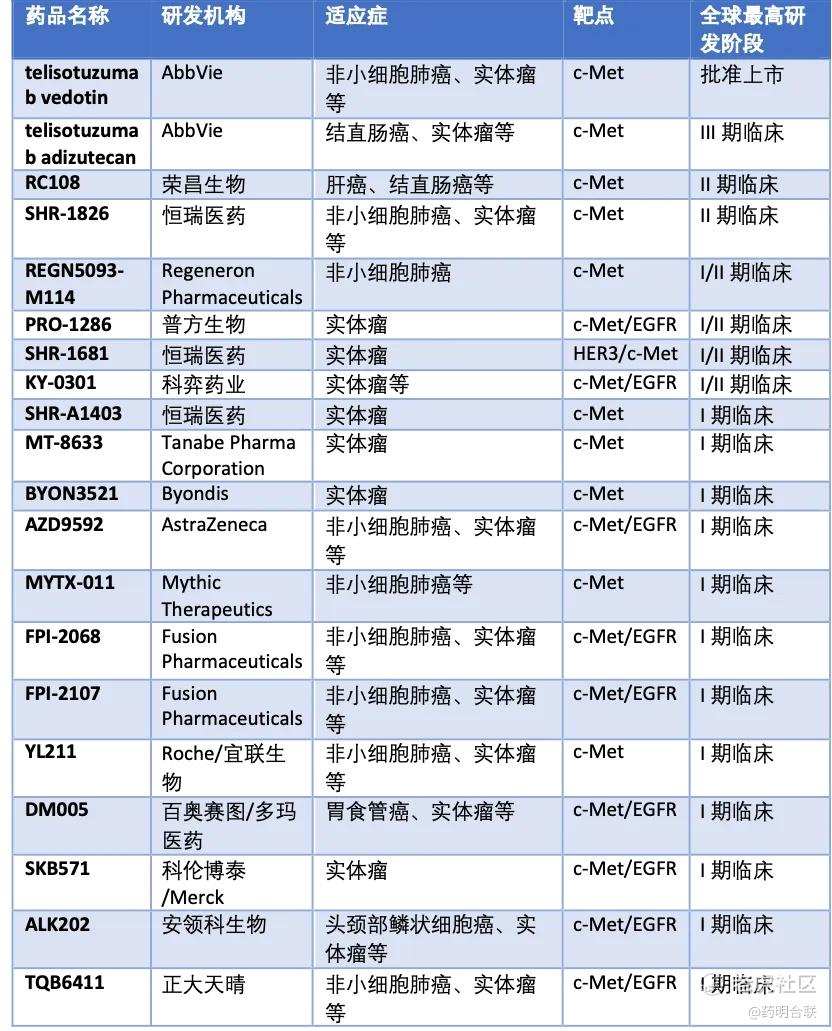
在BD交易方面,根据医药魔方数据显示,目前共有7款c-Met 靶向的ADC药物达成BD交易,如下表所示。c-Met ADC领域研发活跃且市场潜力巨大,BD交易多为国内授权国外MNC,彰显了国际市场对中国创新药的认可。
全球c-Met ADC药物BD交易一览
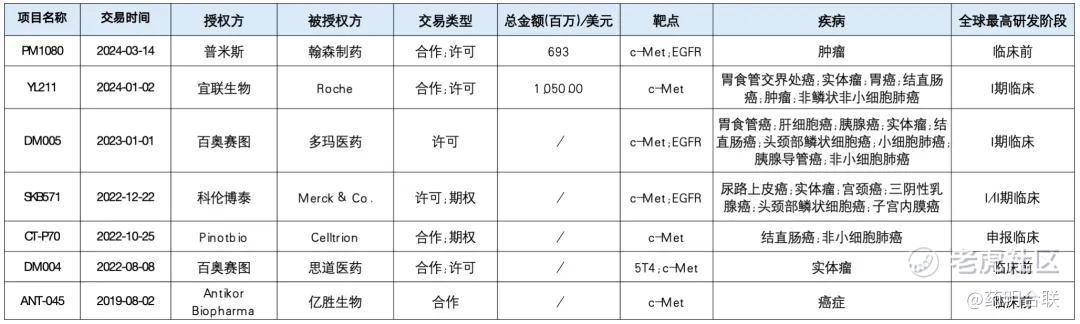
从跨国药企布局来看,罗氏(Roche)于2024年获得宜联生物c-MET ADC(YL211)项目在全球范围内的开发、制造和商业化的独家权益,首付款及近期里程碑付款5000万美元,另外还有近10亿美元的开发、注册和商业化潜在里程碑付款,以及未来基于全球年度销售净额的梯度特许权使用费;阿斯利康(AstraZeneca)的AZD9592(EGFR/c-Met双抗ADC)试图破解奥希替尼耐药问题;强生(J&J)正在探索c-Met疗法在消化肿瘤中的应用;默沙东 (MSD) 就科伦博泰SKB571 c-Met/EFGR ADC产品SKB571的大中华区外全球权益行使选择权并支付3750万美元现金,后续还有开发和销售里程碑金额,以及一定比例的销售分成。
c-Met ADC药物:市场突破与临床进展亮点
Teliso-V(商品名Emrelis) 避开了与小分子TKI的正面交锋,聚焦“无驱动基因突变”的野生型NSCLC患者,此前暂无针对MET扩增/过表达NSCLC患者的药物获批。准确的市场定位有助于药物获得更好的市场表现。艾伯维选择“无驱动基因突变”的野生型NSCLC患者作为第一项适应症,市场规模可观。据Globoldata预测,预计Emrelis销售收入将于2029年达到约5亿美金。据Evaluate Pharma预测,c-Met ADC全球峰值销售额可达30亿美元。
Teliso - V的Ⅱ期LUMINOSITY试验
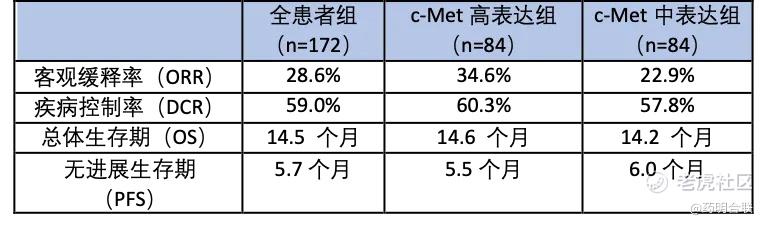
与此同时,艾伯维还在推进一项名为TeliMET NSCLC-01的全球随机、验证性III期临床试验,进一步评估Emrelis作为单药疗法治疗既往接受过治疗的c-Met过表达NSCLC患者的效果。该研究目前正在全球临床试验中心进行患者入组。根据药渡数据库,目前该项III期研究中也纳入了中国患者,试验的主要结果预期将于2028年5月披露。联用方面,艾伯维还正在探索Emrelis与奥希替尼联用的疗效,试图将适应症扩展至EGFR突变人群,进一步扩大市场覆盖。
国内临床进展最快的是恒瑞的SHR-1826和荣昌生物的RC-108, 均处于临床II期阶段:
-
SHR-1826的I 期临床试验结果在2025 ASCO大会上披露。研究表明,SHR-1826在MET变异的晚期实体瘤患者中具有良好抗肿瘤活性和可控安全性:在58例可评估的NSCLC患者中,客观缓解率(ORR)达39.7%,疾病控制率(DCR)达94.8%,安全性可控。
除SHR-1826外,恒瑞医药积极布局c-Met靶点,目前恒瑞已进入临床阶段的有SHR-1816 (c-Met)、SHR-1681 (HER3/c-Met)、SHR-A1403 (c-Met)三个分子。
-
荣昌生物在RC-108的开发上正积极探索联用策略,如RC-108联合信迪利单抗(PD-1)、以及RC-108联合伏美替尼(EGFR-TKI),以进一步验证和优化其临床应用。荣昌生物同样在2025年ASCO大会上公布了RC-108联合伏美替尼在EGFR-TKI治疗失败的局部晚期或转移性非小细胞肺癌(NSCLC)患者的Ib/Ⅱ期研究数据,结果显示了RC-108与伏美替尼的强协同作用:在MET免疫组化(IHC)≥1+且≤20%肿瘤细胞呈胞质3+强染色的患者中,客观缓解率(ORR)为40.5%,中位无进展生存期(PFS)为7.1个月; 在MET IHC≥3+且≤20%肿瘤细胞呈胞质3+强染色的患者中,ORR为61.1%,中位PFS为8.2个月。
结语
Teliso - V的获批为EGFR野生型非鳞状NSCLC中c-Met过表达的患者带来了新的治疗选择。为c-Met 靶点ADC做了一个很好的示范作用。从技术创新层面看,ADC技术的成功应用为c-Met靶点带来了新的活力,激励更多药企投入到c-Met ADC的研发中。适应症扩展方面,目前对于c-Met ADC适应症研究已拓展至胃癌、结直肠癌等。首个c-Met ADC的获批将提振国内外药企对开发c-Met ADC的信心,更多临床的进展仍有待更多药企持续挖掘。
Reference:
各公司官网
医药魔方数据库
ASCO 2025
https://news.qq.com/rain/a/20250515A091TJ00
https://finance.sina.com.cn/stock/thirdmarket/2025-05-22/doc-inexmwyx1634481.shtml
https://news.qq.com/rain/a/20250515A06CV100
https://mp.weixin.qq.com/s/WgDNgHyImnB8-CG4Dg4Iyw
https://mp.weixin.qq.com/s/TD_sBcCgTBrJShkpQswl6Q
https://www.xianjichina.com/special/detail_575905.html
免责声明:合联科讯内容团队专注分享全球生物偶联药行业的科学信息,解读技术创新,传递专家论谈。本文仅作信息交流之目的,文中观点不代表药明合联立场,亦不代表药明合联支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
精彩评论